题目内容
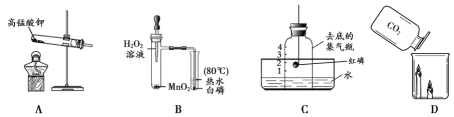
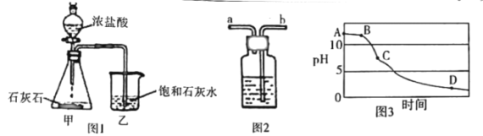
【题目】某兴趣小组用图 Ⅰ装置进行实验时发现.烧杯中饱和石灰水先变浑浊,后逐渐澄清。
(1)写出图1中甲装置中发生反应的化学方程式_______;石灰水变浑浊是因为生成了_______。(填化学式)
(2)为探究“饱和石灰水浑浊后变澄清的原因”,小组开展了如下活动:
[查阅文献]碳酸钙(碳酸钠等)与二氧化碳、水反应生成可溶于水的碳酸氢钙(碳酸氢钠等)
[提出假设]假设1:挥发出的HCl使浑浊变澄清;
假设2:_________。
[设计实验]为除去CO2中的HCl,小华在图1中甲、乙装置之间增加图2装置,装置的连接顺序是甲→____→_____→乙(填字母序号);其中存放的试剂合理是______(填选项序号)。
A 浓硫酸
B 饱和NaHCO3溶液
C 饱和Na2CO3溶液
D NaOH溶液
[实验现象]饱和石灰水浑浊后,继续通入足量CO2,沉淀部分溶解但最终并未完全澄清.
[得出结论]由以上探究可得出结论是_________。
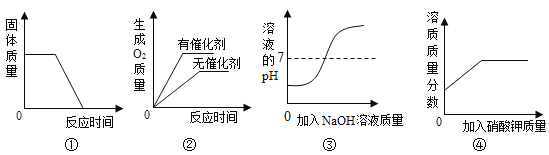
(3)该兴趣小组在老师指导下,用pH传感器测得图1烧杯中溶液的pH随通入时间的变化曲线如图3。
①AB段pH值几乎不变的可能原因是_____; D点所得溶液的成分除H2O外还有_________。
②BC段发生反应的化学方程式主要有_______。
【答案】![]() CaCO3 生成的 CO2 使浑浊变澄清 b a B 挥发出来的氯化氢使石灰水产生的浑浊最终变澄清;二氧化碳只能使石灰水生成的沉淀部分溶解,不能最终使其变澄清 一开始排出来的是空气,不会使溶液的PH值明显变化 CaCl2和HCl
CaCO3 生成的 CO2 使浑浊变澄清 b a B 挥发出来的氯化氢使石灰水产生的浑浊最终变澄清;二氧化碳只能使石灰水生成的沉淀部分溶解,不能最终使其变澄清 一开始排出来的是空气,不会使溶液的PH值明显变化 CaCl2和HCl ![]()
【解析】
(1)由图可知,图1中甲装置中发生的反应是石灰石中的碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,故反应的化学方程式写为:CaCO3+2HCl=CaCl2+H2O+CO2↑。
图1乙装置中的反应是甲装置中生成的二氧化碳与乙装置中的澄清石灰水中的氢氧化钙反应生成水和碳酸钙沉淀,碳酸钙沉淀使澄清石灰水变浑浊,碳酸钙的化学式为CaCO3,故填CaCO3。
(2)[提出假设]由查阅文献可知:碳酸钙能与二氧化碳、水反应生成可溶于水的碳酸氢钙,所以饱和石灰水浑浊后变澄清的原因还有可能是甲中生成的二氧化碳与碳酸钙反应生成可溶性碳酸氢钙的缘故,故填生成的 CO2 使浑浊变澄清。
[设计实验]除去气体中的杂质,应该使气体与洗液充分接触,则气体应该从长管进入洗瓶,所以装置的连接顺序是甲→b→a→乙,故填:b、a;
A 浓硫酸具有吸水性,只能吸收气体中的水分,不会吸收HCl,且不与HCl反应,选项错误;
B NaHCO3能与HCl反应生成NaCl、H2O、CO2,能将杂质转化为欲保留的物质,选项正确
C Na2CO3能与CO2、H2O反应生成可溶于水的NaHCO3,会消耗CO2,选项错误;
D NaOH既能与HCl反应,还能与CO2反应,不符合除杂原则,选项错误,故填:B。
[得出结论]由图1实验可知,浓盐酸挥发出来的氯化氢使石灰水产生的浑浊最终变澄清,向饱和石灰水中通入CO2,饱和石灰水变浑浊后继续通人足量CO2,沉淀部分溶解但最终并未完全澄清,说明二氧化碳只能使石灰水生成的沉淀部分溶解,不能最终使其变澄清,故填:挥发出来的氯化氢使石灰水产生的浑浊最终变澄清;二氧化碳只能使石灰水生成的沉淀部分溶解,不能最终使其变澄清。
(3)①B段pH值几乎不变是因为图甲装置中一开始排出来的是空气,二氧化碳的含量少,反应的氢氧化钙的质量较少,不会使溶液的pH值明显变化,故填:一开始排出来的是空气,不会使溶液的pH值明显变化;
由图可知,D点时溶液的pH<5,溶液呈酸性,这是因为从甲中浓盐酸中挥发出来的氯化氢进入乙中与水形成盐酸,盐酸与氢氧化钙反应生成氯化钙和水,最终盐酸有剩余使溶液呈酸性,所以D点所得溶液的成分除H2O外还有CaCl2和HCl,故填:CaCl2和HCl。
②由图可知,BC段发生反应使溶液由碱性转化为酸性,发生的反应是从甲中浓盐酸中挥发出来的氯化氢进入乙中与水形成盐酸,盐酸与氢氧化钙反应生成氯化钙和水,故反应的化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案