题目内容
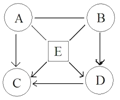
【题目】已知A、B、C、D、E均为初中化学常见的酸、碱、盐。其中A为胃酸的主要成分,B是碱,C是生理盐水的组成成分,E在工业上广泛应用于玻璃、造纸等的生产。将它们配成溶液后,存在如右图所示的转化关系,已知A和E能反应产生气体,请回答下列问题。(“—”表示相互间能反应,“→”表示在某种条件下能生成该物质)
(1)写出A、E的化学式:A ,E ;
(2)写出B与E反应的化学方程式: ;B与E能发生反应的原因是 ;
(3)如果用另一种化合物来代替C,其它物质和条件不变,也符合如图所示要求,那么这种化合物的化学式是 。
【答案】(1)A:HCl E:Na2CO3
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH 生成物有沉淀,反应物都可溶
(3)H2O
【解析】
试题分析:A为胃酸的主要成分,说明A是盐酸, C是生理盐水的组成成分,说明C是氯化钠,E在工业上广泛应用于玻璃、造纸等的生产,说明E是碳酸钠,且B是一种碱,能够和E反应,说明B是氢氧化钙,带入后合题。B与E反应的化学方程式:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;B与E能发生反应的原因是生成物有沉淀,反应物都可溶。如果用另一种化合物来代替C,其它物质和条件不变,也符合如图所示要求,那么这种化合物的化学式是水,因为酸碱盐的反应中都能生成的物质可能是水。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】铜镁合金具有优良的导电性,常用作飞机天线。现欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜合金20g放入烧杯,将280g稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量记录如下.请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀硫酸质量/g | 70 | 70 | 70 | 70 |
剩余固体质量/g | 18.2 | 16.4 | 14.6 | 13.2 |
(1)合金中铜、镁的质量比.
(2)所加稀硫酸的溶质的质量分数.(写出计算过程)

