题目内容
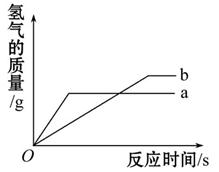
过去的暖气片由铸铁制成,是因为铁具有良好的 性,但它易生锈,所以逐渐被铝合金暖气片取代.铝合金更耐腐蚀,原因是 .金属的广泛用途主要由性质决定,如图是某同学设计的实验,他想要探究的问题是 ,其中发生反应的化学方程式为 . 
导热;在常温下,铝就易与空气中的氧气反应,生成一层致密而坚固的氧化铝薄膜,起保护作用;铁、铜、银三种金属的活动性强弱;Fe+CuSO4=FeSO4+Cu
解析试题分析:暖气片是用来取暖的,铁具有良好的导热性,这是人们利用了热传递的原理来获得热量.
后来,由于铁易生锈,用化学性质比较活泼的铝来代替,是因为在常温下,铝就易与空气中的氧气反应,生成一层致密而坚固的氧化铝薄膜,起保护作用.
根据“在金属活动性顺序中,只有排在前面的金属才能把排在后面的金属从它的盐溶液中置换出来,铁排在铜的前面,而银排在铜的后面”可以知道铁片能与硫酸铜溶液反应置换出铜,而银片不能与硫酸铜溶液反应,所以同学设计的实验能够探究出铁、铜、银三种金属的活动性强弱.
考点:金属的物理性质及用途;金属的化学性质;书写化学方程式、文字表达式、电离方程式.
点评:金属是生活中常见的化学物质,训练学生利用所学金属的性质回答问题的能力,此类型的题目也是近几年中考的热点问题之一.

金属材料在生产、生活中有广泛的用途.
(1)黄铜是铜、锌合金,下列说法中不正确的是 。
| A.黄铜属于纯净物 | B.黄铜属于金属材料 |
| C.黄铜的硬度比铜大 | D.黄铜的抗腐蚀性能更好 |
(3)在 CuCl2和 MgCl2的混合溶液中,加入过量的铁粉,充分反应后过滤,所得固体为 。
根据下图四个化学实验,回答问题:(提示:Cu与Zn的合金称为黄铜)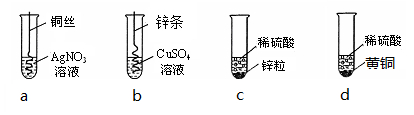
(1)描述实验a中的实验现象 。
(2)要证明Cu、Zn、Ag的活动性顺序,必须要做的实验是 (填实验序号)。
(3)在c实验后的剩余溶液中,一定有的溶质是 ,可能有的溶质是 ,为了确定可能有的溶质,可加入 (填选项序号)
Ⅰ.氯化钡溶液 Ⅱ.氢氧化铜 Ⅲ.氢氧化钠溶液 Ⅳ.锌粒
(4)为了测定d中稀硫酸的溶质质量分数,取20g该黄铜样品于烧杯中,向其中分4次加入该稀硫酸,充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
| | 加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) |
| 第1次 | 25 | 16.75 |
| 第2次 | 25 | 13.5 |
| 第3次 | 25 | m |
| 第4次 | 25 | 12.0 |
试回答下列问题:
Ⅰ.上述表格中m的值为 ;
Ⅱ.该稀硫酸的溶质质量分数是多少?(根据化学方程式计算)