题目内容
【题目】如图是某燃煤发电厂处理废气的装置流程示意图。

(1)从烟囱排出的气体主要成分是_________(至少写2种)。
(2)此过程中S元素的化合价___________(填“有”或“没有” )发生改变。
(3)使用此废气处理装置是为了减少哪种环境问题的形成?_____________。
(4)排出的固体废渣中可以在本流程中循环利用的物质是_____________。
(5)写出反应室中CaO、SO2、O2发生反应的化学方程式:_____________。
【答案】氮气、氧气 有 酸雨 碳酸钙 ![]()
【解析】
(1)根据图示进行分析,燃煤中含有硫,燃烧后生成二氧化硫、二氧化碳,二氧化碳和石灰乳反应生成碳酸钙和水,二氧化硫和氧化钙、氧气反应生成硫酸钙,所以排出的气体主要是氮气,氧气;
(2)此过程中,硫元素的化合价由+4变为+6,故填:有;
(3)经过此废气处理减少了二氧化硫的排放,从而减少了酸雨的形成;
(4)石灰乳吸收二氧化碳生成了碳酸钙和水,碳酸钙在该过程中可以循环使用;
(5)在反应室中CaO、 SO2、 O2发生反应生成硫酸钙,反应的化学方程式为:![]() 。
。

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案【题目】寒假期间,某兴趣小组同学对“锌与硫酸反应快慢的影响因素”进行探究。
[提出问题] 锌与硫酸反应的快慢与哪些因素有关?
[猜想假设](1)a、可能与锌的形状、颗粒大小有关;
b、可能与硫酸的质量分数大小有关;
c、还可能与______有关。
[设计与实验] 以3分钟内收集到的氢气体积作为判断依据,具体如下表所示:
实验 编号 | 锌的形状 (均取1 g) | 硫酸的浓度 (均取20 mL) | 氢气的体积 (/mL) |
① | 锌粒 | 20% | 31.7 |
② | 锌片 | 20% | 50.9 |
③ | 锌粒 | 30% | 61.7 |
④ | 锌片 | 30% |
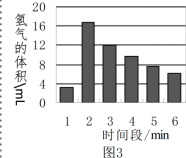
[比较分析](2)要验证猜想a ,可选择的实验编号是_______________。
(3)实验④由于没有及时记下数据,经同学回忆,你认为比较可能的数值是__________(填“57.5”或“75.5”)。
[得出结论](4)完成实验①②③后,可以得出影响该反应快慢的一条结论是:________。
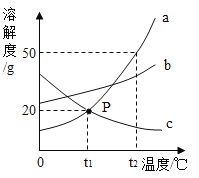
[反思评价] 图3是用实验①来测定,在每一分钟内收到氢气的体积变化图,请
(5)第1分钟时间内反应的速率较慢,这是由于锌粒表面有些氧化膜(ZnO)覆盖,则其原因用化学方程式表示为______。
(6)从第3分钟开始,反应的速率又逐渐变______,这是因为______。
【题目】对比学习有利于发现事物的共性与个性。为探究酸的性质,同学们进行了如下实验。
实验内容 | 实验现象 | 分析与结论 |
| 醋酸晶体试管内___,醋酸溶液试管中镁带表面冒气泡。 | 酸的很多反应通常在水溶液中才能完成。 |
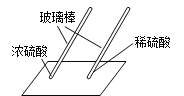
用玻璃棒蘸硫酸在白纸上写字 | _______(填“浓”或“稀”)硫酸使白纸炭化。 | 即使是同种酸,由于____不同,它们的性质不完全相同。 |
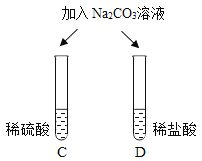
| 两试管中均产生_____ | 不同的酸具有相似的性质,这是因为酸的组成中都含有_____(填元素符号)。 |
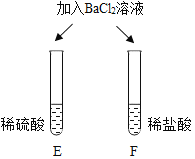
| E试管中产生_____, F试管中无明显现象。 | 不同的酸根会导致酸的“个性”差异。因此,可用氯化钡溶液鉴别盐酸和硫酸。 |
清洗试管时,小乔同学将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀。请分析上述现象并回答:
Ⅰ.废液缸中产生气体的化学方程式为______。
Ⅱ. 废液缸里最终产生的白色沉淀中一定有硫酸钡,可能有____(填化学式)。