题目内容
【题目】有100g碳酸钙,高温煅烧一段时间后,剩余固体的质量为67g。下 列推断不符合客观事实的是
A.生成CO2的质量是33g
B.生成物中CaO的物质的量是0.75mol
C.剩余固体中钙元素的质量分数大于40%
D.剩余固体中碳元素与氧元素的质量之比大于1:4
【答案】D
【解析】
A、由质量守恒定律可知,反应生成的CO2的质量=100g-67g=33g,故A 正确;
B、设生成物中CaO的质量是x,
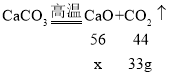
![]() x=42g,生成物中CaO的物质的量
x=42g,生成物中CaO的物质的量![]() ,故B 正确;
,故B 正确;
C、碳酸钙中钙元素的质量分数=![]() ,由于反应后部分碳酸钙转化为氧化钙,过程中固体中钙元素的质量不变,但固体的质量减小,所以剩余固体中钙元素的质量分数大于40%,故C 正确;
,由于反应后部分碳酸钙转化为氧化钙,过程中固体中钙元素的质量不变,但固体的质量减小,所以剩余固体中钙元素的质量分数大于40%,故C 正确;
D、碳酸钙中碳元素与氧元素的质量之比=12:(16×3)=1:4,反应过程中碳元素全部转化为二氧化碳,氧元素只有部分转化,生成的氧化钙中不含有碳元素,所以剩余固体中碳元素与氧元素的质量之比小于1:4,故D错误。故选D。

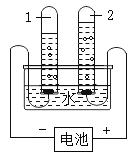
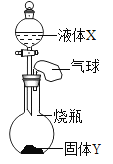
【题目】如图所示,将一定量的液体 X 滴入到烧瓶中,若小气球先鼓起,一段时间后又变瘪(液体 X的体积忽略不计),则液体 X 和固体 Y 是( )
选项 | 液体X | 固体Y |
A | 水 | 氧氧化钠 |
B | 水 | 碳酸铵 |
C | 过氧化氢溶液 | 二氧化锰 |
D | 稀盐酸 | 碳酸钠 |
A.AB.BC.CD.D
【题目】校化学兴趣小组欲对市售的某些牙背、牙粉进行探究。以下是A牙膏、B牙膏、C牙粉商标上摩擦剂的主要成分。
A牙膏 | B牙膏 | C牙粉 |
氢氧化铝、碳酸钙 | 碳酸钙 | 碳酸钙 |
查阅资料:氢氧化铝固体既能与酸反应生成盐和水,也能和碱反应生成盐和水(牙膏和牙粉中除了摩擦剂以外,其它物质均不与酸、碱反应)。
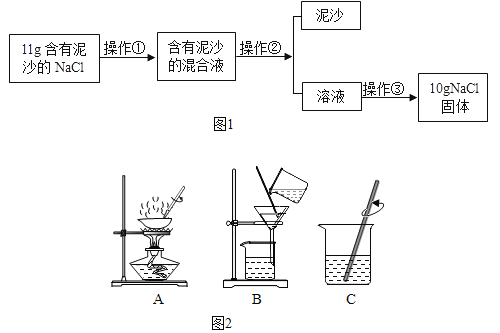
实验一:验证 A牙膏中含有氢氧化铝、碳酸钙,实验设计如下:

(1)步骤②中x的具体操作过程是_____。
(2)从步骤③的探究结果可知A牙膏中一定含有碳酸钙摩擦剂,原因用化学方程式表示为_____。
(3)为进一步证明氢氧化铝存在,向过滤所得沉淀中加入_____,当观察到_____,可以证明氢氧化铝存在。
实验二:比较B 牙膏和C牙粉中碳酸钙含量的多少,实验设计如下:
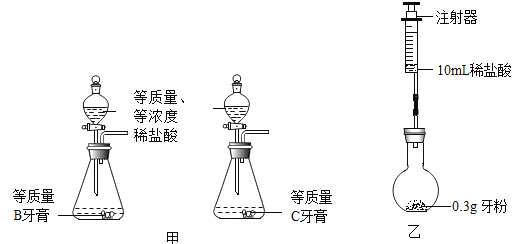
步骤 | 实验操作 | 实验现象 |
① | 用同一套装置先后进行两次实验,装入药品如图甲 | |
② | 打开分液漏斗活塞注入一定量稀盐酸,然后关闭活塞 | 有气泡产生 |
③ | 待②反应结束后,再打开分液漏斗活塞,注入一定量稀盐酸,然后关闭活塞 | 无明显现象 |
④ | 称量反应后装置及药品的总质量并比较 | 加入B牙膏的装置及药品的总质量大于加入C牙粉的装置及药品的总质量 |
(4)实验结论为_____。
(5)步骤③的作用是_____。
(6)有同学认为该实验前可以不检查装置的气密性,你是否认同?并说明原因_____。
实验三:测定C牙粉中碳酸钙的含量
(7)方案一:若不改动实验二的装置和基本步骤,要测定牙粉中碳酸钙的质量分数,还应测定的数据有_____。
(8)方案二:取C牙粉0.3g放入图乙装置,再将注射器中10mL稀盐酸迅速压入烧瓶中。实验记录如下:
时间/min | 1 | 3 | 5 | 7 | 8 | 9 | 10 |
注射器读数/mL | 40.0 | 59.0 | 60.0 | 60.4 | 60.5 | 60.5 | 60.5 |
综合分析以上实验过程和数据,最终生成气体的体积是_____mL。根据气体体积计算其质量,进而计算C牙粉中碳酸钙的含量。