题目内容
【题目】水是生命之源。请回答下列问题:
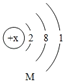
(1)矿物质水中元素及国标含量如图所示。

①矿物质水中含有的氯离子_____;(填符号,下同)
②硫酸镁中镁元素的化合价为+2价_____;
③钠_____(填“属于”或“不属于”)人体所需的微量元素。
(2)有些农村打深井取用地下水,可用_____(填物质名称)区分地下水是软水还是硬水,生活中常用_____的方法来降低水的硬度。
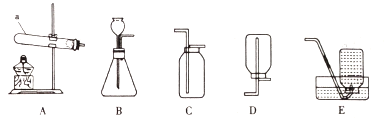
(3)小华制作了一个过滤器,想把水中的悬浮颗粒除去。那么你认为在组装过滤装置时,玻璃仪器有:烧杯、玻璃棒、_____;其中玻璃棒作用是_____。
(4)如图是活性炭净水器示意图,则正确的是_____(填字母序号)。
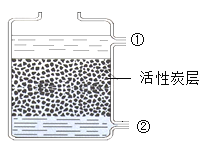
A ①处是出水口,②处是入水口
B ①处是入水口,②处是出水口
(5)北京某自来水厂净水过程如图所示:
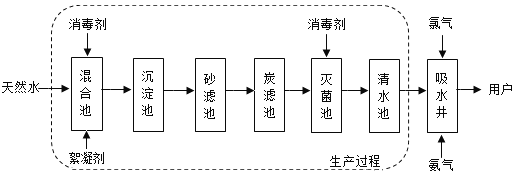
①炭滤池中常用煤粉替代活性炭,这说明煤粉具有的性质是_____。
②自来水生产过程中,使用的净水方法除①中涉及到的还有_____(填序号)。
a沉淀 b过滤 c煮沸 d蒸馏 e杀菌消毒
③吸水井中通入的氯气和氨气可生成氯胺。氯胺可缓慢释放出具有消毒作用的物质。这步操作的目的是_____(填序号)。
a对天然水消毒 b对生产过程中的水消毒 c对输往用户的水消毒
【答案】Cl- ![]() 不属于 肥皂水 加热煮沸 漏斗 引流 A 吸附性 abe c
不属于 肥皂水 加热煮沸 漏斗 引流 A 吸附性 abe c
【解析】
(1)①矿物质水中含有的氯离子带一个单位负电荷:Cl-;
②硫酸镁中镁元素的化合价为+2价:![]() ;
;
③钠元素不属于人体所需的微量元素。
(2)有些农村打深井取用地下水,可用肥皂水区分地下水是软水还是硬水,生活中常用加热、煮沸的方法来降低水的硬度。
(3)小华制作了一个过滤器,想把水中的悬浮颗粒除去。在组装过滤装置时,玻璃仪器有:烧杯、玻璃棒、漏斗;其中玻璃棒作用是引流,防止液体飞溅。
(4)由活性炭净水器示意图,下端②为进水口,上端①为出水口,故选:A;
(5)①炭滤池中常用煤粉替代活性炭,这说明煤粉具有疏松多孔状结构,有吸附性;
②自来水生产过程中,使用的净水方法除①中涉及到的还有:a沉淀、b过滤、e杀菌消毒;
③吸水井中通入的氯气和氨气可生成氯胺。氯胺可缓慢释放出具有消毒作用的物质。这步操作的目的是:c对输往用户的水消毒

【题目】空气中氧气含量测定的再认识,某化学兴趣小组的同学,在实验室用红磷、木炭等物质代替汞对空气中氧气的含量测定进行模拟探究。
(实验1)A组同学通过燃烧红磷法测定空气中氧气的含量,写出红磷燃烧的符号表达式:_____。
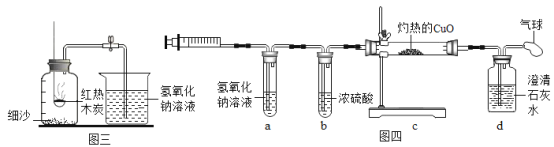
(实验2)B组”利用木炭燃烧测定空气中氧气的体积分数”,根据经验,利用如图三装置测定空气中氧气含量时,能否用木炭替代?_____(填“能”或“不能”)。
(提供资料)
氢氧化钠能与二氧化碳反应生成碳酸钠和水。该小组同学选择用氢氧化钠溶液吸收生成的二氧化碳气体(如图三),但进入集气瓶中水的体积分数仍然小于![]() 。
。
(提出问题)是什么原因导致测量不准确呢?
(猜想与假设)他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;丙同学:可能是木炭与空气反应生成了其他气体。
(查阅资料)
资料一:木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数分别高达14.0%,8.0%和16.0%。
资料二:木炭在密闭容器中不充分燃烧会生成一氧化碳气体。
资料三:一氧化碳能与灼热的氧化铜粉末(黑色)反应生成铜(红色)和二氧化碳气体
(探究一)小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,可知_____同学的猜想不合理。
(探究二)乙同学又利用上述装置设计了如下实验,请你填写下表:
实验步骤 | 实验现象 | 实验结论 |
①将足量木炭点燃,迅速插入装有氧气的 集气瓶中 | ________ | 木炭燃烧没有消耗完集气瓶中的氧气 |
②待装置冷却后,将燃着的_____ (填“棉花”或“蜡烛“)再伸入集气瓶中 | _________ |
(探究三)小明从木炭燃烧产物的角度猜想还可能是生成了_____导致测量结果小于1/5;于是用注射器抽取集气瓶内的气体做了上图(图四)所示的实验,当观察到d中_____(填实验现象),可证明小明的猜想成立。
(经典对比)通过与上述实验对比如图,拉瓦锡选择用汞的优点有_____。
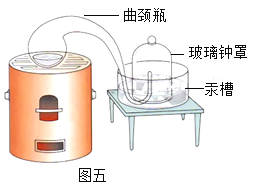
A能将密闭装置内空气中的氧气几乎耗尽
B在汞槽中起到液封作用
C实验过程中没有污染
D生成的化合物加热分解又能得到汞和氧气
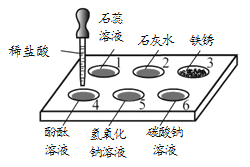
【题目】某兴趣小组活动中,同学们按图1装置对“可燃物燃烧的条件”进行探究,探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问。
(查阅资料)白磷的着火点是40℃,红磷的着火点是240℃,燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,并能与空气中的水蒸气反应,生成有毒的偏磷酸(H2PO3)。
(交流与讨论)白烟对人体健康有害,该实验装置必须改进。
(改进与实验)同学们按改进后的图2装置进行实验。
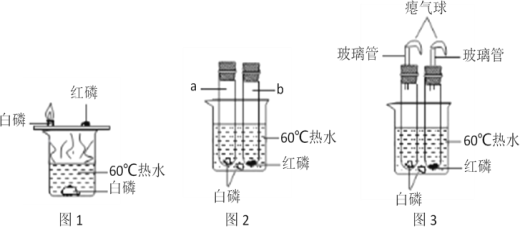
请你帮助他们将下表补充完整。
实验现象 | 对实验现象的解释 |
a试管中白磷燃烧,热 水中白磷没有燃烧 b试管中红磷没有燃烧 | (1)热水中白磷没有燃烧的原因是___________ (2)b试管中红磷没有燃烧的原因是________ |
(反思与评价)
(3)改进后的图2装置与图1装置比较的优点是___________。
(4)小雅同学指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是___________。
(5)检查完装置的气密性之后,小实进行了上述实验。实验小结时,小实同学认为还可以用冷却后的a试管测定空气中氧气的含量,他的操作是___________最终发现进入a试管内液体的体积小于试管容积的![]() ,如果不考虑橡皮塞占试管的容积,出现这种现象的原因可能是________。
,如果不考虑橡皮塞占试管的容积,出现这种现象的原因可能是________。
【题目】小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
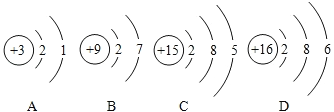
(提出猜想)除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。
(完成实验)按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度 |
① | KClO3 | 580℃ |
② | KClO3、MnO2(质量比1:1) | 350℃ |
③ | KClO3、CuO(质量比l:1) | 370℃ |
④ | KClO3、Fe2O3(质量比1:1) | 390℃ |
(分析数据、得出结论)
(1)由实验__________与实验④对比,证明猜想合理;
(2)实验所用的三种金属氧化物,催化效果最好的是____________。
(3)若Fe2O3是该反应的催化剂,请写出这个反应的文字表达式___________。
(4)如表是二氧化锰用量与一定质量氯酸钾制取氧气反应速率关系的实验数据。
二氧化锰与氯酸钾的质量比 | 1:40 | 1:20 | 1:10 | 1:5 | 1:3 | 1:2 |
生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 |
①据如表可知二氧化锰与氯酸钾的质量比为_______________时,反应速率最快
②通过分析可知,在化学反应中催化剂的用量____________越多越好 (填“是”或“不是”);
③二氧化锰用量过多冲淡了氯酸钾粉末,相当于减少反应物的________,所以反应速率受到影响。