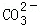题目内容
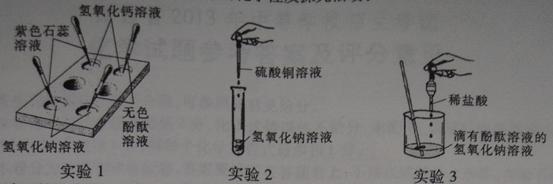
小强同学用三支试管,分别取适量的稀盐酸、澄清石灰水、碳酸钠溶液,进行相关实验探究。
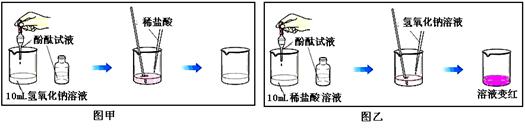
步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,说明Na2CO3溶液显_____性;
步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含有________。
(选填答案:A.稀盐酸 B.澄清石灰水 C.碳酸钠溶液)
[实验猜想] 步骤3所得滤液中溶质可能为:
①NaCl Na2CO3; ②NaCl CaCl2和NaOH; ③NaCl Na2CO3和NaOH; ④……
[实验验证](提示:CaCl2溶液显中性)
[反思评价] 有同学提出将CaCl2溶液改为稀盐酸,若观察到有气泡产生且红色消失,则证明猜想③成立。小刚同学认为不正确,其理由是:___________________________。
步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,说明Na2CO3溶液显_____性;
步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含有________。
(选填答案:A.稀盐酸 B.澄清石灰水 C.碳酸钠溶液)
[实验猜想] 步骤3所得滤液中溶质可能为:
①NaCl Na2CO3; ②NaCl CaCl2和NaOH; ③NaCl Na2CO3和NaOH; ④……
[实验验证](提示:CaCl2溶液显中性)
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入足量CaCl2溶液 | | 猜想③成立 |
[反思评价] 有同学提出将CaCl2溶液改为稀盐酸,若观察到有气泡产生且红色消失,则证明猜想③成立。小刚同学认为不正确,其理由是:___________________________。
碱 A 现象:有白色沉淀生成且红色不消失 理由:无法证明氢氧化钠存在
步骤1:酚酞呈红色说明溶液显碱性
步骤3:因混合后有白色沉淀生成且溶液显红色,即溶液仍呈碱性,所以滤液中一定不含稀盐酸(酸性)
实验现象 由于猜想3中的Na2CO3可与CaCl2反应生成白色的CaCO3沉淀,且氢氧化钠不反应溶液还应呈碱性,因此溶液还会呈红色。
反思评价: 加稀盐酸若有气泡产生可说明含Na2CO3,但红色消失不能说明原溶液中是否含氢氧化钠。如原溶液中只含有Na2CO3发生的现象也相同。
点评:科学探究题目要注意实验现象前后的对应性和严谨性。
步骤3:因混合后有白色沉淀生成且溶液显红色,即溶液仍呈碱性,所以滤液中一定不含稀盐酸(酸性)
实验现象 由于猜想3中的Na2CO3可与CaCl2反应生成白色的CaCO3沉淀,且氢氧化钠不反应溶液还应呈碱性,因此溶液还会呈红色。
反思评价: 加稀盐酸若有气泡产生可说明含Na2CO3,但红色消失不能说明原溶液中是否含氢氧化钠。如原溶液中只含有Na2CO3发生的现象也相同。
点评:科学探究题目要注意实验现象前后的对应性和严谨性。

练习册系列答案
相关题目