题目内容
某校研究性学习小组进行了一个有趣的实验探究:
《提出问题》实验室有一瓶久置的NaOH,变质程度怎样?
《设计方案》先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3
的质量,从而进一步确定样品中NaOH的质量分数。
《进行实验》实验测得加入稀盐酸的质量与产生CO2气体的质量关系如下图所示。
《数据处理》写出以下计算过程: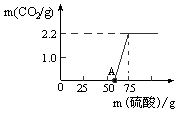
(1)该样品中Na2CO3的质量为多少?(2分)
(2)该样品中NaOH的质量分数为多少?(2分)
《反思与交流》①从图中0~A点说明:在NaOH 与Na2CO3的混合溶液中,加入强酸,首先反应的物质是 ;②根据反应方程式分析,NaOH部分变质或全部变质,与没有变质的NaOH相比,中和反应时消耗强酸的量 。
《提出问题》实验室有一瓶久置的NaOH,变质程度怎样?
《设计方案》先称取21.2g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入一定质量分数的稀硫酸直至过量,根据生成CO2的质量计算出Na2CO3
的质量,从而进一步确定样品中NaOH的质量分数。
《进行实验》实验测得加入稀盐酸的质量与产生CO2气体的质量关系如下图所示。
《数据处理》写出以下计算过程:

(1)该样品中Na2CO3的质量为多少?(2分)
(2)该样品中NaOH的质量分数为多少?(2分)
《反思与交流》①从图中0~A点说明:在NaOH 与Na2CO3的混合溶液中,加入强酸,首先反应的物质是 ;②根据反应方程式分析,NaOH部分变质或全部变质,与没有变质的NaOH相比,中和反应时消耗强酸的量 。
《数据处理》
(1)5.3g
(2)75.0%。
《反思与交流》①NaOH ②相同
(1)5.3g
(2)75.0%。
《反思与交流》①NaOH ②相同
由图象可知,在检验样品中的杂质时加入稀硫酸,并无二氧化碳气体产生,原因是在碱性溶液中,硫酸与碱发生中和反应,不产生气体,当加入的硫酸的质量为50g时,开始与样品中的碳酸钠发生反应,生成二氧化碳气体,并随着反应的进行,当继续滴加硫酸时,产生的气体为2.2g,并且不再变化,说明样品中的碳酸钠完全反应完毕,由此可根据二氧化碳的质量计算出样品的碳酸钠的质量,同些也可计算出原样品中氢氧化钠的质量,从而得出样品中氢氧化钠的质量分数.过程如下:
[数据处理]从图中得知:产生CO2的最大量为2.2g.(1分)
(1)解:设该样品中Na2CO3的质量为x,则:
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑(1分)
106 44
x 2.2g
x=(2.2g×106)/ 44 =5.3g(2分)
(2)则样品中NaOH质量分数为:(21.2g-5.3g)/ 21.2g ×100%=75.0%(1分)
答:样品中Na2CO3的质量为5.3g;NaOH的质量分数为75.0%.
[反思与交流]假设碳酸钠先与酸反应,反应时生成二氧化碳,但是生成的二氧化碳接着被氢氧化钠吸收变为碳酸钠,所以推出酸先于氢氧化钠反应;由于变质过程中钠元素不损失也不增加,并且钠元素最终都变为氯化钠,所以可以推出消耗酸的质量相同.
故答案为:NaOH;相同
点评:本题综合考查了学生对图象问题的识别能力,近几年中考题中对此类问题的考查越来越多,解题关键还是要看明确图象所表示的意义,综合性较强,易出错.
[数据处理]从图中得知:产生CO2的最大量为2.2g.(1分)
(1)解:设该样品中Na2CO3的质量为x,则:
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑(1分)
106 44
x 2.2g
x=(2.2g×106)/ 44 =5.3g(2分)
(2)则样品中NaOH质量分数为:(21.2g-5.3g)/ 21.2g ×100%=75.0%(1分)
答:样品中Na2CO3的质量为5.3g;NaOH的质量分数为75.0%.
[反思与交流]假设碳酸钠先与酸反应,反应时生成二氧化碳,但是生成的二氧化碳接着被氢氧化钠吸收变为碳酸钠,所以推出酸先于氢氧化钠反应;由于变质过程中钠元素不损失也不增加,并且钠元素最终都变为氯化钠,所以可以推出消耗酸的质量相同.
故答案为:NaOH;相同
点评:本题综合考查了学生对图象问题的识别能力,近几年中考题中对此类问题的考查越来越多,解题关键还是要看明确图象所表示的意义,综合性较强,易出错.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 :
: