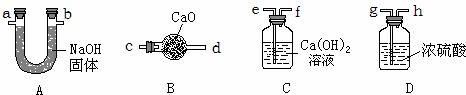题目内容
(1)若用氯酸钾和二氧化锰来制取氧气,该反应的化学方程式为 ,
其中二氧化锰在化学反应前后固体混合物中的质量分数将 。(填“变大”、
“变小”或“不变”)
(2)待固体完全反应后通过以下四步实验操作回收二氧化锰。正确操作的先后顺序是
(填写选项序号)。
a.烘干 b.溶解 c.洗涤 d. 过滤
(3)过滤、蒸发时都需用到的仪器是 (填序号)。
A.酒精灯 B.烧杯 C.玻璃棒 D.漏斗 E.量筒
(4)小丽想要用回收的氯化钾配制50 g 10℅的氯化钾溶液。

配制该溶液的操作步骤
①计算:需要氯化钾固体的质量为 g,水 mL(水的密度近似看作1g/cm3 )
 ②称量:用托盘天平称取所需固体,再用 mL的量筒量取所需的水;
②称量:用托盘天平称取所需固体,再用 mL的量筒量取所需的水;
③溶解:将称得的氯化钾固体放入烧杯中,再倒入量取的水,用玻璃棒充分
搅拌;
④装瓶:将配制的溶液倒入试剂瓶,并贴上标签。请在装有所配制溶液的试
剂瓶(见右图)标签上标明相应信息。
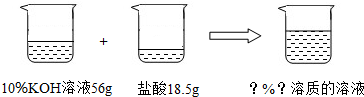
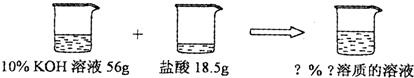
(5)如下图所示,已知一定质量分数、一定质量的氢氧化钾溶液与一定质量的盐酸恰好
完全反应。求算反应后溶液的溶质质量分数。

(1) 2KClO3![]() 2KCl+3O2↑ 变大 (每空1分,共2分)
2KCl+3O2↑ 变大 (每空1分,共2分)
(2)bdca (1分)
|
(4)①5 45 ②50 ④ (4分)
(5)解:56gKOH溶液中KOH的质量为56g×10%=5.6g
设反应后生成KCl的质量为x
KOH + HCl = KCl +H2O (1分)
56 74.5
5.6g x
56∶74.5 = 5.6g∶x
x=7.45g (1分)
![]() 反应后所得溶液中溶质质量分数为: 7.45g (1分)
反应后所得溶液中溶质质量分数为: 7.45g (1分)
74.5g
(其它合理解法均可给分)
答:反应后溶液的溶质质量分数为10%。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案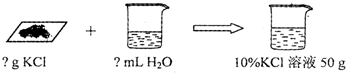


 (3)若要得到干燥的CO2,图(一)还需要一个干燥装置,干燥剂为浓硫酸.图(二)画出了该干燥装置的一部分,请你补充画出其它部分,并用箭头标明气体进出方向.
(3)若要得到干燥的CO2,图(一)还需要一个干燥装置,干燥剂为浓硫酸.图(二)画出了该干燥装置的一部分,请你补充画出其它部分,并用箭头标明气体进出方向.


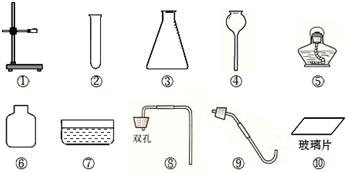 26、实验室提供了以下仪器,请你随某兴趣小组的同学一起来参加实验探究活动:
26、实验室提供了以下仪器,请你随某兴趣小组的同学一起来参加实验探究活动: