题目内容
【题目】根据下列实验装置图,回答有关问题:

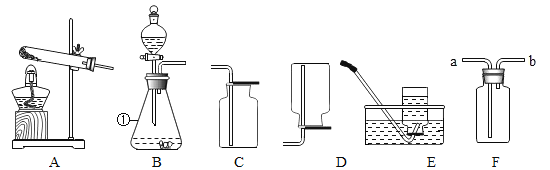
(1)实验室常用锌粒和稀硫酸反应制取氢气,若要控制产生氢气的速率,应选择的发生装置是___(从A﹣F中选填字母),写出反应的化学方程式____;
(2)实验室现用G装置制取二氧化碳气体。
①检查装置的气密性:关闭活塞K,将干燥管放入带有水的烧杯中,若观察到____,则表明该装置的气密性良好。
②将装有石灰石的干燥管放入装有稀盐酸的烧杯内,同时打开活塞K,干燥管内发生反应的化学方程式为___,一段时间后,关闭导管上的活塞K,反应停止,其原理是___。该装置的优点是___。
【答案】C; Zn+H2SO4=====ZnSO4+H2↑ 干燥管中液面低于烧杯中液面; CaCO3+2HCl=====CaCl2+H2O+CO2↑; 关闭活塞 K 后,干燥管内由于继续反应生成 CO2 气体,使得装置内气压大于外界大气压, 将干燥管内液体排至烧杯中,使石灰石和稀盐酸完全分离,反应结束 可以控制反应的开始与停止。
【解析】
(1)制取氢气是用锌与稀硫酸反应,反应物的状态是固体和液体,不需要加热,可选用的发生装置是B或C,C中注射器可以控制液体的滴加速度,所以要控制产生氢气的速率,应选择的发生装置是C,锌和稀硫酸反应生成硫酸锌和氢气,化学方程式为:Zn+H2SO4═ZnSO4+H2↑;
(2)①检验装置气密性利用装置内外的压强差检验,所以关闭活塞K,将干燥管放入带有水的烧杯中,若观察到干燥管中液面低于烧杯中液面,则表明该装置的气密性良好;
②碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;一段时间后,关闭导管上的活塞K,反应停止,原理是:关闭活塞K后,干燥管内由于继续反应生成CO2气体,使得装置内气压大于外界大气压,将干燥管内液体排至烧杯中,使石灰石和稀盐酸完全分离,反应结束,该装置的优点是:可以控制反应的开始与停止。

 阅读快车系列答案
阅读快车系列答案