题目内容
化学方程式的书写是化学学习的基本技能.下列化学方程式书写正确的是( )A.H2CO3═CO2↑+H2O
B.4P+5O2
 2P2O5
2P2O5C.Zn+HCl═ZnCl2+H2↑
D.Fe+CuSO4═Cu↓+FeSO4
解答:解:A、该化学方程式书写完全正确.
B、该化学方程式反应条件应为点燃,正确的化学方程式为:4P+5O2
 2P2O5.
2P2O5.C、该化学方程式没有配平,正确的化学方程式应为:Zn+2HCl═ZnCl2+H2↑.
D、该化学方程式反应物中铁是固体,铜的后面不需要标注↓,正确的化学方程式应为Fe+CuSO4═Cu+FeSO4.
故选A.
点评:本题难度不大,在解此类题时,首先分析应用的原理是否正确,然后再根据方程式的书写规则进行判断,化学方程式正误判断方法是:先看化学式是否正确,再看配平,再看反应条件,再看气体和沉淀,最后短线改成等号.

人类社会的发展离不开能源。当今社会,人类利用的能源主要来自化石燃料。(1)用来驱动汽车、飞机和轮船的燃料主要是从石油中根据不同沸点范围分馏出来的汽油、航空煤油、柴油等,石油分馏的过程属__________变化。化石燃料中主要含有碳、氢元素,完全燃烧的产物是_____________,还含有硫、氮等元素,燃烧时会转化为_________________。
(2)西气东输,将改变我市居民的气体燃料结构。下表是几种气体燃料的价格和热值:
|
燃烧物 |
煤气 |
液化石油气 |
天然气 |
|
价格 |
1.4元/千克 |
6.0元/千克 |
1.8元/千克 |
|
热值 |
1.56×104kJ/kg |
4.5×104kJ/kg |
3.9×104kJ/kg |
综合考虑,你将选用哪种燃料 理由是________________ 。
(3)化石燃料不仅是优质的能量资源,还是宝贵的化工资源。聚乙烯是一种最常用的塑料,它是以石油裂解气体乙烯(CH2=CH2)为原料,经许多乙烯分子打开双键(-CH2-CH2-)连在一起,聚合成大分子而形成的。下图是聚乙烯分子形成过程的示意图,卡通画中单个小人代表一个乙烯分子。聚乙烯其中的部分结构可表示为:… …。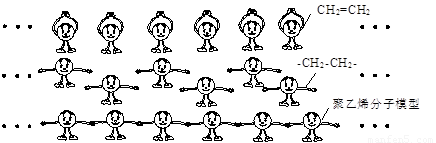
(4)开发和利用清洁高效而又用之不竭的新能源,是21世纪人类面临的重要课题。①2006年1月起,我省苏北四市推广使用乙醇汽油。乙醇可利用农作物发酵制得,农作物在催化剂作用下转化为葡萄糖(C6H12O6),然后葡萄糖在酒化酶的作用下转化为乙醇和二氧化碳,写出葡萄糖转化为乙醇的化学方程式 _________ 。
②氢气是一种未来理想的能源。现通过生物法制得的氢气中混有CO2、O2和水蒸气等(氢气的体积分数通常为60℅~90℅),为了得到纯净的氢气,将混合气体依次通过NaOH溶液、灼热的Cu丝和干燥装置。该除杂方案是否正确? ,理由是
。
【解析】(1)没有新物质生成的变化属于物理变化,含有碳、氢元素的物质完全燃烧能生成水和二氧化碳,含有的硫、氮等元素,燃烧时会转化为二氧化硫和氮的氧化物;
(2)可以通过计算单位价格购买的热量来选择燃料.
(3)本题是一信息给予题,通过题中信息进行分析解答.
(4)①书写化学方程式时首先要正确写出反应物和生成物的化学式,然后配平,再注明反应条件.
②除去一种气体中的其他杂质时,要选择适当的物质并注意除杂的顺序,还有除杂过程中可能发生的反应等.当氢气和氧气混合遇到高温或明火时有可能发生爆炸.
 柠檬酸为无色半透明晶体,无臭、味极酸,易溶于水和乙醇,在潮湿空气中易潮解.
柠檬酸为无色半透明晶体,无臭、味极酸,易溶于水和乙醇,在潮湿空气中易潮解.