题目内容
柠檬酸为无色半透明晶体,无臭、味极酸,易溶于水和乙醇,在潮湿空气中易潮解.水溶液显酸性,加热可以分解成多种产物,与酸、碱等发生反应.主要用于香料或作为饮料的酸化剂.(1)上述划线部分属于柠檬酸的
(2)柠檬酸(C6H8O7)在氧气中完全燃烧的化学方程式:
(3)工业上柠檬酸由蔗糖发酵制得,发生的主要反应为:
C12H22O11+3 A→2C6H8O7+3H2O,A的化学式是
(4)食品加工业中,可以用压制柑橘所得汁液作为提取柠檬酸的原料.提取过程如下:
①原料提取:柑橘汁液中有不少果胶及固体杂质,需进行初步提纯,自然沉降后用压滤机进行
②中和:在①所得原料澄清液中加入石灰浆,至溶液呈青绿色时,即表示已完成中和反应.然后静置沉淀,此沉淀即为果酸钙(以柠檬酸钙为主). 若用H3R表示柠檬酸的化学式,请书写该中和反
应的化学方程式
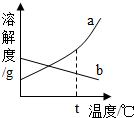
③除盐:所得柠檬酸钙中含有某种盐分,可用70~80℃热水洗涤,反复多次,直至盐分除净为止.请根据操作分析该盐分的溶解度曲线可能是右图中

④酸解脱色:柠檬酸钙浆液与浓度为35%的硫酸充分反应,静置沉淀,上层清液为柠檬酸溶液,此反应属于
的柠檬酸用
98%的浓硫酸(密度为1.84g/mL)
⑤浓缩结晶:将不饱和柠檬酸液进行恒温浓缩结晶.在此过程中,保持不变的是
a.溶液中溶剂的质量 b.柠檬酸的溶解度
c.溶液中溶质的质量分数 d.溶液和晶体中柠檬酸总质量.
分析:(1)根据化学性质的概念(物质在化学变化中所表现出来的性质)回答
(2)根据质量守恒定律来书写
(3)根据质量守恒定律反应前后原子个数相等来回答
(4)①根据过滤的原理、方法回答;②根据酸碱中和反应的原理③根据“用70~80℃热水洗涤,反复多次,直至盐分除净”来判定;④根据复分解反应的概念、活性炭的作用、根据溶液稀释溶质质量不变来计算;⑤根据溶解度的概念
(2)根据质量守恒定律来书写
(3)根据质量守恒定律反应前后原子个数相等来回答
(4)①根据过滤的原理、方法回答;②根据酸碱中和反应的原理③根据“用70~80℃热水洗涤,反复多次,直至盐分除净”来判定;④根据复分解反应的概念、活性炭的作用、根据溶液稀释溶质质量不变来计算;⑤根据溶解度的概念
解答:解:(1)根据化学性质的概念可确定;故答案为:化学
(2)C6H8O7在氧气中完全燃烧可确定生成物为水和二氧化碳;故答案为:2C6H8O7+9O2
8H2O+12CO2
(3)根据质量守恒定律反应前后原子个数相等;故答案为:O2
(4)①因是不溶性固体与液体的分离;故答案为:过滤
②根据中和反应中氢离子与氢氧根离子的个数相等来配平;故答案为:2H3R+3Ca(OH)2=Ca3R2+6H2O
③因是热水把盐分洗净故该盐分受温度影响较大;故答案为:a
④因是盐与酸发生的反应、活性炭具有吸附性;根据溶液稀释溶质质量不变,可计算出需要98%的浓硫酸的体积为:5000g×35%÷98%÷1.84g/mL═970.5mL;故答案为:复分解反应、活性炭、970.5mL
⑤某温度下,物质的溶解度是不变的;同样柠檬酸的总质量保持不变.故答案为:bd.
(2)C6H8O7在氧气中完全燃烧可确定生成物为水和二氧化碳;故答案为:2C6H8O7+9O2
| ||
(3)根据质量守恒定律反应前后原子个数相等;故答案为:O2
(4)①因是不溶性固体与液体的分离;故答案为:过滤
②根据中和反应中氢离子与氢氧根离子的个数相等来配平;故答案为:2H3R+3Ca(OH)2=Ca3R2+6H2O
③因是热水把盐分洗净故该盐分受温度影响较大;故答案为:a
④因是盐与酸发生的反应、活性炭具有吸附性;根据溶液稀释溶质质量不变,可计算出需要98%的浓硫酸的体积为:5000g×35%÷98%÷1.84g/mL═970.5mL;故答案为:复分解反应、活性炭、970.5mL
⑤某温度下,物质的溶解度是不变的;同样柠檬酸的总质量保持不变.故答案为:bd.
点评:此题考查了我们生活中的化学,需要同学们在生活中注意观察分析.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
 柠檬酸为无色半透明晶体,无臭、味极酸,易溶于水和乙醇,在潮湿空气中易潮解.
柠檬酸为无色半透明晶体,无臭、味极酸,易溶于水和乙醇,在潮湿空气中易潮解.

