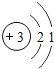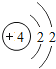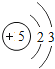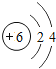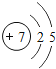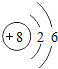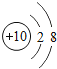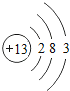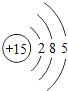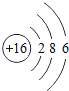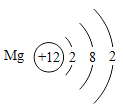题目内容
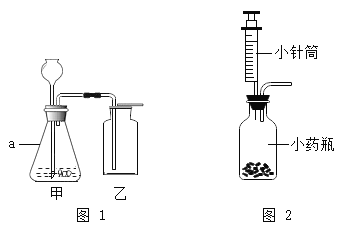
【题目】请从A~D中任选三个实验作答,若均做答,按前三个计分。如下图,在一只集气瓶(或广口瓶)中进行实验。回答相关问题。
序号 | 步骤 | 问题 |
A | ①收集一瓶氧气②伸入燃着的木炭③倒入澄清石灰水并振荡 | 该实验的目的是_______。 |
B | ①收集二氧化碳②倒入氢氧化钠溶液振荡③…… | 该实验探究CO2能否与NaOH反应,步骤③的操作是______。 |
C | ①倒入10%的H2O2溶液②伸入带火星的木条③加入少量MnO2 | 实验的结论是__________。 |
D | ① 放入燃着的蜡烛②放入少量碳酸钙粉末③加入适量盐酸 | 观察到的现象是_______。 |
【答案】利用澄清石灰水来检验木炭和氧气反应的产物是否是二氧化碳 向充分振荡的溶液中滴加稀盐酸 过氧化氢在二氧化锰催化的作用下产生了能使带火星的木条复燃的氧气 燃着的蜡烛逐渐熄灭
【解析】
木炭在氧气中点燃生成二氧化碳,二氧化碳和氢氧化钠反应生成碳酸钠和水,过氧化氢在二氧化锰催化作用下生成水和氧气,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳。
实验A,澄清石灰水遇到二氧化碳会变浑浊,用这一实验现象来检验二氧化碳,A实验的目的是利用澄清石灰水来检验木炭和氧气反应的产物是否是二氧化碳。实验B,要想验证二氧化碳与氢氧化钠是否反应,只需向充分荡振的溶液中滴加稀盐酸,看是否有气泡产生,若有气泡产生,则证明二者能反应,若无气泡产生,则证明二者不能反应。实验C,氧气是助燃剂,该实验通过带火星的木条复燃来证明过氧化氢在二氧化锰催化的作用下能产生氧气,从而根据实验现象得出结论:过氧化氢在二氧化锰催化的作用下可以产生了能使带火星的木条复燃的氧气。实验D,碳酸钙粉末中加入盐酸后会产生二氧化碳气体,而二氧化碳气体不支持燃烧,能使燃着的蜡烛熄灭,观察到的现象为燃着的蜡烛逐渐熄灭。
序号 | 步骤 | 问题 |
A | ①收集一瓶氧气②伸入燃着的木炭③倒入澄清石灰水并振荡 | 该实验的目的是利用澄清石灰水来检验木炭和氧气反应的产物是否是二氧化碳。 |
B | ①收集二氧化碳②倒入氢氧化钠溶液振荡③…… | 该实验探究CO2能否与NaOH反应,步骤③的操作是向充分振荡的溶液中滴加稀盐酸。 |
C | ①倒入10%的H2O2溶液②伸入带火星的木条③加入少量MnO2 | 实验的结论是二氧化锰能加快过氧化氢分解的速率 |
D | ① 放入燃着的蜡烛②放入少量碳酸钙粉末③加入适量盐酸 | 观察到的现象是白色固体减少或消失,有大量气泡产生,燃着的蜡烛逐渐熄灭。 |

 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案【题目】核电荷数为1﹣18的原子结构示意图等信息如下,请回答下列问题:
第一周期 | 1H
| 2He
| |||||||
第二周期 | 3Li
| 4Be
| 5B
| 6C
| 7N
| 8O
| 9F
| 10Ne
| |
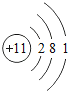
第三周期 | 11Na
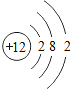
| 12Mg
| 13Al
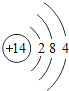
| 14Si
| 15P
| 16S
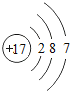
| 17Cl
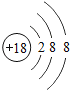
| 18Ar
| |
(1)不同种元素最本质的区别是_____(选填序号)
A质子数不同 B最外层电子数不同 C中子数不同 D相对原子质量不同
(2)在第三周期中,各原子结构的共同之处是_____;该周期中,各原子核外电子排布的变化规律是_____.
(3)在第三周期中,元素类型的变化情况是:从左到右由_____元素过渡到_____元素,并以稀有气体元素结尾.
(4)写出核外电子排布与氖原子相同的阳离子和阴离子各一个:阳离子_____,阴离子_____.
【题目】84消毒液是生活中常用的一种消毒液,主要成分为次氯酸钠(NaClO)。实验小组对其进行研究。
(查阅资料)
Ⅰ. NaClO溶液呈碱性。
Ⅱ.消毒杀菌的原理是使菌体蛋白质变性,变性程度越大,消毒液消毒杀菌效果越好。鸡蛋清中的蛋白质发生变性反应时变为白色固体物质。
Ⅲ.ORP指84消毒液的漂白能力,ORP数值越大,84消毒液的漂白能力越强。
(进行实验)
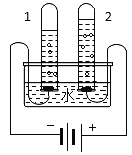
实验1:制备84消毒液
某同学制作了一种84消毒液发生器(如图所示),用石墨作电极,电解饱和氯化钠溶液,即可制得消毒液。

实验2:在鸡蛋清中加入不同浓度的消毒液,静置15min现象如下表。
序号 | 2-1 | 2-2 | 2-3 | 2-4 |
实验 操作 |
|
|
|
|
实验现象 | 液体表面产生大量气泡,无其他现象 | 液体中产生大量白色固体 | 液体中产生少量白色固体 | 液体中产生极少量白色固体 |
实验3:探究84消毒液漂白性的影响因素
序号 | 3-1 | 3-2 |
实验操作 | 取烧杯倒入30mL浓度为1:100的84消毒液,将烧杯放置在距离光源 10cm处进行光照,测量ORP变化 | 取四个烧杯,分别倒入30mL浓度为1:100的84消毒液,并置于20°C、30°C、40°C、50°C水浴中加热,测量 ORP变化 |
测量数据 |
|
|
(解释与结论)
(1)实验1中,发生的主要反应如下,补全①的化学方程式。
①2NaCl+2H2O![]() 2NaOH+ Cl2↑+______ ↑ ②Cl2+2NaOH =NaCl+NaClO+H2O
2NaOH+ Cl2↑+______ ↑ ②Cl2+2NaOH =NaCl+NaClO+H2O
(2)实验2的目的是_______。
(3)实验3-1的结论是_______。
(4)根据实验3-2的测量数据可知,影响84消毒液漂白性的因素有_________。
(反思与评价)
(5)由实验3可知,84消毒液储存时需注意________。
(6)生活中,84消毒液不能与洁厕灵(主要成分是盐酸)混合使用的原因是________。