题目内容
【题目】钙元素是人体必需的元素。请根据图回答问题:
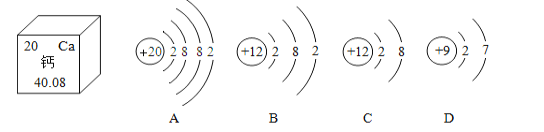
(1)钙原子最外层电子数是___;
(2)钙元素的相对原子质量为___;
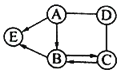
(3)A、B、C、D表示的微粒中属于同一种元素的是___(填字母序号);
(4)在B、C、D中与A具有相似化学性质的微粒是___(填字母序号);
(5)氢化钙(CaH2)是一种制取氢气的原料,在氢化钙中氢元素的化合价是__;氢化钙与水反应生成氢气和一种碱,该反应的化学方程式为___。
【答案】 2; 40.08; BC; B; -1 CaH2+2H2O===Ca(OH)2+2H2↑
【解析】
(1)由图可知,钙元素的原子序数为20,钙原子最外层电子数为2;
(2)根据钙元素在元素周期表中的信息,钙元素的相对原子质量为40.08;
(3)元素的种类由质子数决定,因为BC的质子数相同,所以BC属于同种元素的粒子;
(4)最外层电子数相同的粒子具有相似的化学性质,A粒子的最外层有2个电子,B粒子最外层也有2个电子,它们的化学性质相似;
(5)钙元素通常显示+2价,根据化合物中化合价的代数和为0可求得,CaH2中氢元素的化合价是-1价,氢化钙和水反应生成氢氧化钙和氢气,故反应方程式为CaH2+2H2O===Ca(OH)2+2H2↑。

【题目】如表是 NaCl、NH4Cl 在不同温度时的溶解度。
温度/℃ | 0 | 20 | 40 | 60 | 80 | |
溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | |
(1)以上两种物质的溶解度受温度影响较大的是_____。
(2)40℃时,将 40.6g NaCl 加入到 100g 水中,充分搅拌使之溶解,所得溶液的质量为_____g。
(3)20℃时,NaCl 饱和溶液的溶质质量分数为(精确到小数点后 1 位)_____。