题目内容
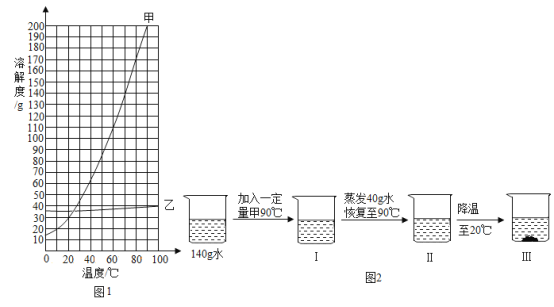
【题目】下图为三种物质的溶解度曲线。下列说法错误的是
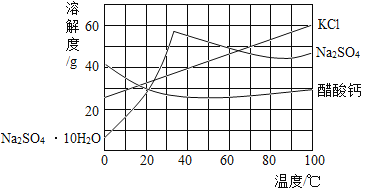
A.约在64℃时KCl和Na2SO4的溶解度相等
B.在室温至100℃区间,随温度升高,Na2SO4的溶解度先增大后减小,醋酸钙则相反
C.分离含少量KCl的Na2SO4溶液,采用先蒸发浓缩,后降温结晶的方法
D.在40℃时,40gKCl固体溶于60g水得到40%KCl溶液
【答案】D
【解析】
A、据图可以看出,约在64℃时KCl和Na2SO4的溶解度相等,选项正确;
B、据图可以看出,在室温至100℃区间,两者的溶解度随温度变化趋势相反,选项正确;
C、在温度高于某温度时,硫酸钠的溶解度随温度升高而减小,低于该温度时,硫酸钠的溶解度随温度降低而减小,而氯化钾的溶解度随温度升高一直增大,但受温度的影响较小,分离含少量KCl的Na2SO4溶液,采用先蒸发浓缩,后降温结晶的方法,选项正确;
D、在40℃时,氯化钾的溶解度为40g,40gKCl固体在60g水中不能全部溶解,故不能得到40%的溶液,选项错误。
故选D。

 名校课堂系列答案
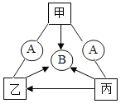
名校课堂系列答案【题目】右图所示,某河旁甲、乙、丙、丁四座化工厂排放的工业废水中分别含有碳酸钠、氯化铜、氢氧化钠、盐酸中的一种.某同学对①、②、③、④处水质监测时记录了以下现象.根据现象推断,甲、乙、丙、丁四座化工厂排放工业废水的成分,错误的是( )
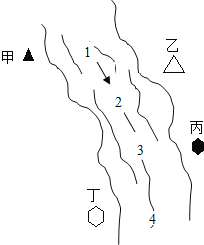
① | ② | ③ | ④ | |
记录现象 | 无色溶液 | 蓝色浑浊 | 浑浊消失 | 产生气泡 |
A.甲:碳酸钠 B.乙:氯化铜 C.丙:盐酸 D.丁:碳酸钠
【题目】在过氧化氢溶液的分解反应中,某化学兴趣小组发现:除了二氧化锰,硫酸铜溶液也能对H2O2的分解起催化作用。对此,他们进行了有关探究。
(提出问题)CuSO4溶液是混合物,是其中哪一种成分起到了催化作用呢?
(查阅资料)①稀硫酸中主要含有H2O、H+、SO42三种微粒。
②CuSO4溶液中主要含有H2O、Cu2+、SO42三种微粒。
(作出猜想)根据以上信息,同学们作出了如下三个猜想:
Ⅰ:SO42催化分解H2O2 Ⅱ:Cu2+催化分解H2O2 Ⅲ:H2O催化分解H2O2
(1)其中,明显不合理的是_______(填序号),理由是_______。
(实验验证)
(2)为了验证自己的猜想,同学们设计了如下两个实验(所取H2O2溶液的浓度相同):
操作 | 现象 | 结论 |
取5 mL H2O2溶液于试管中,滴入少量的稀硫酸,伸入带火星的木条 | _______ | SO42对H2O2的分解不起催化作用 |
_______ | 产生大量气泡,带火星的木条复燃 | _______ |
(实验拓展)
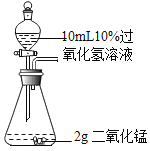
实验一:用图甲装置探究影响H2O2分解速率的因素,得到图乙、图丙所示曲线(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计)。
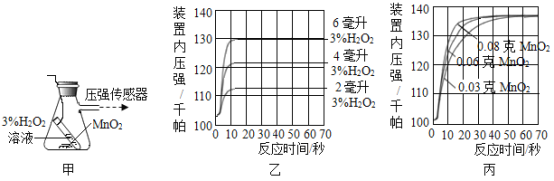
(3)写出图甲中反应的化学方程式_______。
(4)图乙是“0.1 g MnO2与不同体积的3% H2O2溶液混合”的实验结果,从图中可以看出_______。
(5)图丙是用“8 mL浓度为3%的H2O2溶液与不同质量的MnO2混合”时,所得到的曲线,通过该曲线可以得到的结论是_______。
实验二:用图丁装置探究氧气的浓度对燃烧的影响。点燃蜡烛后立即塞紧橡皮塞,待蜡烛熄灭后,将滴管中的水全部滴入瓶中,铝盒中的白磷燃烧。
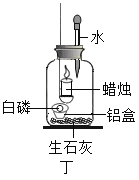
(6)白磷燃烧的主要现象是_______。
(7)由“蜡烛熄灭,白磷燃烧”可得出的结论是_______。
(8)滴入水后白磷燃烧的原因是_______。
【题目】请完成下列实验,回答问题。
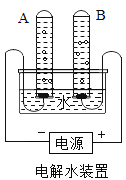
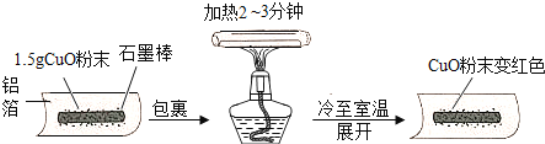
(1)通过水的电解认识水:
①宏观现象:按图所示装置,通电一段时间后,试管A、B中产生气体的体积比约为_______。
②微观该反应中发生分解的微粒名称是___________。
③结论:水由_________组成。
(2)下列依据实验目的所设计的实验操作中,正确的是_______(可能有多个正确选项)
选项 | 实验目的 | 实验操作 |
A | 除去CO2混有HCl气体 | 将气体通过足量NaOH溶液 |
B | 鉴别NH4Cl和KCl两种白色固体肥料 | 加入熟石灰研磨后闻气味 |
C | 检验生石灰中是否有未分解的石灰石 | 滴加稀盐酸观察现象 |
D | 除去二氧化碳中的一氧化碳 | 将气体点燃 |