题目内容
【题目】将盛有等质量、等质量分数且足量的稀盐酸的两只烧杯,放在托盘天平的左右两盘,天平平衡.在左盘烧杯中加入10克碳酸钙,若要使天平重新平衡,则右盘烧杯中应加入的物质可能是( )
A.10克碳酸钾和碳酸钠 B.10克碳酸镁和碳酸钠
C.5.5克氧化铜 D.10克镁粉和铜粉
【答案】B
【解析】
试题设左边烧杯中产生的二氧化碳的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
10g x
![]()
x=4.4g
左边烧杯的质量增加量为:10g﹣4.4g=5.6g,也就是说右边烧杯的质量增加量也为5.6g天平才能保持平衡.
A、由于碳酸钙的相对分子质量是100,所以要想在加入10g碳酸盐的混合物生成的二氧化碳也是4.4g,必须是两种碳酸盐的相对分子质量一个大于100另一个小于100,而碳酸钾的相对分子质量是138、碳酸钠的相对分子质量是106,都大于100,故该选项错误;
B、由A的分析进行判断,碳酸镁的相对分子质量是84、碳酸钠的相对分子质量是106,所以加入10克碳酸镁和碳酸钠有可能使天平平衡;
C、氧化铜与盐酸反应不会生成气体,所以加入5.5克氧化铜则右盘会增重5.5g,所以天平不会平衡;
D、由于镁与盐酸反应能生成氢气,而铜不能与盐酸反应,假设该金属全部是镁,设生成氢气的质量是y
Mg+2HCl═MgCl2+H2↑
24 2
10g y
![]()
y=0.83g
故不管是镁铜以何种比例混合右盘的增重一定大于5.6g;天平不能平衡;
故选B

 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案【题目】以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格(包括表中的空格)。
(提出问题)化学反应前后各物质的质量总和是否相等?
(猜想与假设)猜想1:不相等; 猜想2:相等。
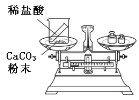
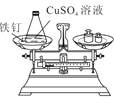
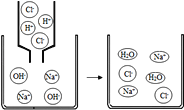
(实验探究)甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲 组 | 乙 组 | |
实验方案(反应后略) |
|
|
实验现象 | 有气泡产生, 天平指针向右偏转 | 铁钉表面有红色物质析出, 溶液颜色发生改变, 天平指针没有偏转 |
结论 | 猜想1正确 反应的化学方程式:____ | 猜想2正确 |
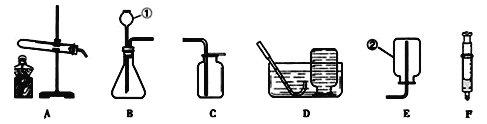
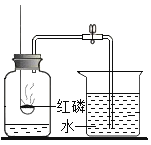
(反思评价)究竟哪种猜想正确?通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在_____中进行。
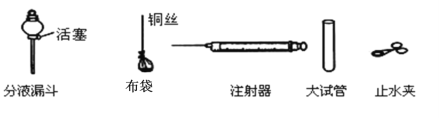
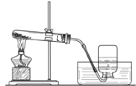
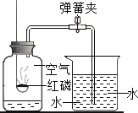
(优化装置)同学们对甲组左盘中的反应装置进行了如下两种改进,你认为最佳装置是_______(填序号)。
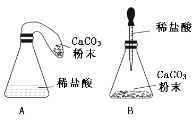
(得出结论)同学们利用改进后的最佳装置进行再次探究,均得出猜想二正确。最终得出结论是:_____的各物质的质量总和等于反应后生成的各物质的质量总和。
(解释应用)解释:化学反应前后,原子的种类、数目、质量均不变,所以质量守恒。
【题目】请从A或B两题中任选1个作答,若两题均作答,按A计分。
A | B |
(1)该反应的化学方程式为_____。 (2)用排水集气法收集O2的原因 是______。 |
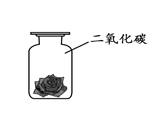
将紫色石蕊溶液浸泡并晾干的小花,一半喷水后放入集气瓶中,实验的现象是______,该实验中主要化学方程式是______。 |