题目内容
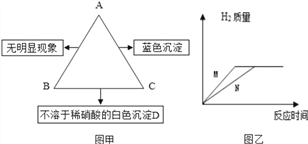
【题目】有A,B,C三种物质,已知A是一种氯化物,B是一种酸,C是一种碱.图甲表示A、B、C三种物质的溶液两两混合时的实验现象,请回答:
(1)D的化学式为______________;
(2)A、C反应的化学方程式为____________;
(3)将一定质量镁、锌两种金属同时放入A溶液中充分反应,过滤、滤液为无色,则滤液中一定含有的阳离子为_______(写粒子符号);
(4)若M、N分别为铁和锌中的一种,分别与等质量、等溶质质量分数的B溶液反应,产生氢气的质量与反应时间的关系如图乙所示,反应结束后只有一种金属有剩余,则剩余金属为_____。
【答案】 BaSO4 Ba(OH)2 + CuCl2 = Cu(OH)2 ↓ + BaCl2 Mg 2+ Fe
【解析】(1)A,B,C三种物质,A是一种氯化物,B是一种酸,C是一种碱,A和C反应会生成蓝色沉淀,C和B反应会生成不溶于酸的白色沉淀,所以A是氯化铜,C是氢氧化钡,B是硫酸,经过验证,推导正确,所以D是氢氧化钡和硫酸生成的硫酸钡沉淀,化学式为:BaSO4;(2)A、C的反应是氯化铜和氢氧化钡反应生成氢氧化铜沉淀和氯化钡,化学方程式为:Ba(OH)2 + CuCl2 = Cu(OH)2 ↓ + BaCl2;(3)将一定质量镁、锌两种金属同时放入氯化铜溶液中,镁会先与氯化铜反应,锌再与氯化铜反应,所以充分反应,过滤、滤液为无色,滤液中一定含有的阳离子为Mg2+;(4)若M、N分别为铁和锌中的一种,分别与等质量、等溶质质量分数的稀硫酸溶液反应,则金属全部参加反应,产生氢气的质量一样,产生氢气的质量M快,所以M金属活泼,则M为锌,生成等质量的氢气需要的铁的质量小于锌的质量,每65份质量的锌会生成2份质量的氢气,每56份质量的铁会生成2份质量的氢气,所以反应结束后只有一种金属有剩余,则剩余金属为铁。

【题目】某补钙剂说明书的部分信息如图所示,现用20片该药剂制成的固体粉末与40g稀盐酸混合(其他成分不与盐酸反应),稀盐酸平均分成4次加入烧杯中,实验数据见下表:

实验序号 | 加入稀盐酸的质量/g | 固体粉末剩余质量/g |
1 | 10 | 18.9 |
2 | 10 | 17.8 |
3 | 10 | 16.8 |
4 | 10 | m |
(1)该瓶补钙剂属于__________。(填物质分类)
(2)表格中的m=________。
(3)求稀盐酸的浓度____________。(请根据化学方程式写出完整的计算步骤)
(4)该瓶补钙剂含有碳酸钙________g。(结果保留1位小数)
(5)请根据上述内容,在下图中补全图像。
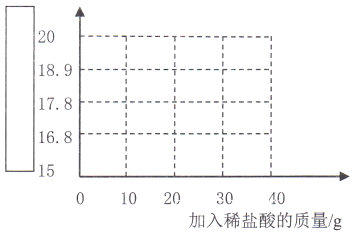 ___________
___________
【题目】兴趣小组同学对“氢氧化钠溶液与稀硫酸混合是否发生了化学反应”进行了如下探究:
【提出问题】氢氧化钠溶液与稀硫酸混合是否发生了化学反应?
【猜想与假设】
a:二者混合发生了化学反应;
b:二者混合没有发生化学反应。
【设计并实验】
实验操作 | 实验现象 | |
甲同学 | 向盛有10mL一定溶质质量分数的氢氧化钠溶液的烧杯中,用胶头滴管慢慢滴入1-2滴稀硫酸,振荡,同时测定溶液的pH | 溶液pH减小但仍大于7 |
乙同学 | 向盛有10mL一定溶质质量分数的氢氧化钠溶液的烧杯中,先滴入几滴无色酚酞试液,然后再加入稀硫酸 | 溶液由红色变为无色 |
【得出结论】氢氧化钠溶液与稀硫酸发生了化学反应。
(1)乙同学认为甲的实验设计不合理,原因是_____________,改进的方法是____________;根据改进后的实验现象说明二者混合后发生了化学反应,写出氢氧化钠溶液与稀硫酸反应的化学方程式__________;甲同学也认为乙的实验设计也不合理,你是否赞同,说出你的理由___________。
【思考与交流】
丙同学在绝热装置中,向分别盛有10mL10%氢氧化钠溶液加入不同体积某浓度的稀硫酸,充分混合后溶液的温度变化曲线如图(混合前稀硫酸和氢氧化钠溶液均为18℃)。
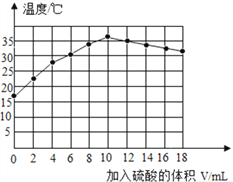
(2)根据图示分析,稀硫酸和氢氧化钠的反应是__________(填吸热、放热)反应,加入稀硫酸_________mL时,二者恰好完全反应.