题目内容
【题目】根据下列装置,结合所学化学知识回答下列问题:
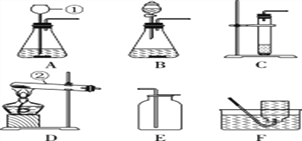
(1) 写出图中标号仪器的名称:① _______。
(2) 实验室用高锰酸钾制取氧气时,发生装置应选用________(填字母);其反应的化学方程式为__________________________。如果改用氯酸钾和二氧化锰制取氧气,反应前后二氧化锰的质量分数________(填“增大”、“减小”或“不变”)。
(3) 实验室制取少量二氧化碳时,发生装置最好选用________(填字母,下同),收集装置选用________,常用此收集方法的原因是____________________,某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊,可能的原因______________________________________________
(4) 化学反应可控制才能更好地为人类造福,我们可以通过改变反应的条件、药品用量、改进装置等途径来达到控制反应的目的。常温下块状电石(CaC2)与水反应生成乙炔(C2H2)气体和氢氧化钙,该反应的化学方程式是______________________________,实验室制取乙炔时,须严格控制加水速度,以免剧烈反应放热引起装置炸裂。图中适合制取乙炔气体的发生装置有________(填装置序号)。
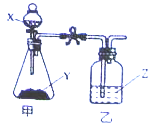
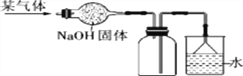
(5)下图是干燥、收集某气体的装置。由实验装置可以推测该气体的有关性质,请你在表中找出相对应的选项(____)
序号 气体性质 | A | B | C | D |
溶于水中所得溶液的pH | >7 | <7 | >7 | <7 |
其密度(ρ1)与空气密度(ρ2)的比较 | ρ1>ρ2 | ρ1>ρ2 | ρ1<ρ2 | ρ1<ρ2 |
在水中的溶解性 | 极易溶 | 难 溶 | 极易溶 | 难 溶 |
【答案】 长颈漏斗 D 2KMnO4![]() K2MnO4+MnO2+O2↑ 增大 C E 密度比空气大 石灰水变质或二氧化碳中混有氯化氢 CaC2+2H2O=C2H2↑+Ca(OH)2 B C
K2MnO4+MnO2+O2↑ 增大 C E 密度比空气大 石灰水变质或二氧化碳中混有氯化氢 CaC2+2H2O=C2H2↑+Ca(OH)2 B C
【解析】(1)①的仪器的名称是:长颈漏斗;(2) 实验室用高锰酸钾制取氧气时,为固体加热型,故发生装置应选用D;高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应的化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;如果改用氯酸钾和二氧化锰制取氧气,反应前后固体质量减少,二氧化锰的质量分数增大;(3) 实验室制取少量二氧化碳时,发生装置最好选用C,收集装置选用E,常用此收集方法的原因是二氧化碳密度比空气大,某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊,可能的原因是:石灰水变质或二氧化碳中混有氯化氢,石灰水变质实验无现象,氯化氢气体溶于水形成盐酸,盐酸和石灰水反应生成氯化钙和水;(4)制取乙炔气体,是在常温下用块状电石与水反应,即固体和液体的反应,又因为该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂,所以应选用装置B,B装置加液体的是注射器,可控制加水的速度,该反应的化学方程式为:CaC2+2H2O=C2H2↑+Ca(OH)2;(5)下图是干燥、收集某气体的装置。由实验装置可知,干燥剂氢氧化钠只能干燥碱性气体,导气管短进长出,说明密度比空气小,极易溶于水,故相对应的选项为C。
K2MnO4+MnO2+O2↑;如果改用氯酸钾和二氧化锰制取氧气,反应前后固体质量减少,二氧化锰的质量分数增大;(3) 实验室制取少量二氧化碳时,发生装置最好选用C,收集装置选用E,常用此收集方法的原因是二氧化碳密度比空气大,某同学取一定浓度盐酸与石灰石反应,将生成的气体通入澄清石灰水中,始终未见浑浊,可能的原因是:石灰水变质或二氧化碳中混有氯化氢,石灰水变质实验无现象,氯化氢气体溶于水形成盐酸,盐酸和石灰水反应生成氯化钙和水;(4)制取乙炔气体,是在常温下用块状电石与水反应,即固体和液体的反应,又因为该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂,所以应选用装置B,B装置加液体的是注射器,可控制加水的速度,该反应的化学方程式为:CaC2+2H2O=C2H2↑+Ca(OH)2;(5)下图是干燥、收集某气体的装置。由实验装置可知,干燥剂氢氧化钠只能干燥碱性气体,导气管短进长出,说明密度比空气小,极易溶于水,故相对应的选项为C。

 考前必练系列答案
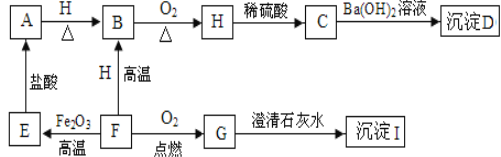
考前必练系列答案【题目】某同学对碳酸钙高温加热一段时间剩余固体的成分进行探究。
(1)写出高温分解的化学方程式________________。
(2)取反应后的少量固体于试管中,加适量水振荡,静置,有不溶物出现,过滤。
(3)向滤渣中滴加过量稀盐酸,有气泡。固体中一定含有_______。
(4)某兴趣小组用图1装置进行实验时发现:烧杯中饱和石灰水未变浑浊,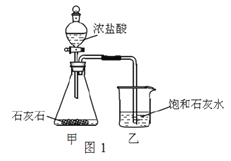
①写出甲装置中发生反应的化学方程式_________________________。
②为探究“饱和石灰水未变浑浊的原因”,开展了如下活动:
分析原因: 可能是澄清石灰水已变质; 也可能是生成的气体中除了有CO2外,还有____________;
实验探究: 将生成的气体X通入图2装置。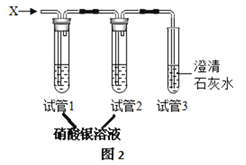
装置 | 试管1 | 试管2 | 试管3 |
现象 | _________ | 无明显变化 | 白色沉淀 |
试管3中发生的化学方程式为_______________;试管2中试剂的作用是_________。