题目内容
【题目】实验室有一瓶未用完的长期敞口放置的氢氧化钠样品(不考虑水的存在),质量是9.3g,与一定质量分数的稀盐酸92.9g恰好完全反应,产生气体的质量为2.2g。试计算完全反应后所得溶液中溶质的质量分数。(写出具体计算过程)__________________
【答案】11.7%
【解析】
解:设样品中碳酸钠的质量为x,其与盐酸反应生成氯化钠的质量为y
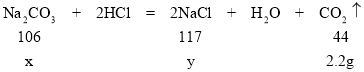
106:44=x:2.2g x=5.3g
117:44=y:2.2g y=5.85g
样品中剩余氢氧化钠的质量为9.3g5.3g=4g
设氢氧化钠与盐酸反应生成氯化钠的质量为z
![]()
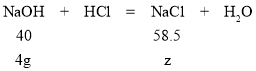
40:58.5=4g:z z=5.85g
完全反应后所得溶液中溶质的质量分数为![]() ×100%=11.7%
×100%=11.7%
答:完全反应后所得溶液中溶质的质量分数为11.7%。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目