题目内容
【题目】(6分)某化工厂排放的废液中含有大量的硫酸锌和硫酸铜,兴趣小组根据所学知识设计了一个方案来回收金属铜并得到硫酸锌晶体,主要过程如图所示,请回答下列问题:
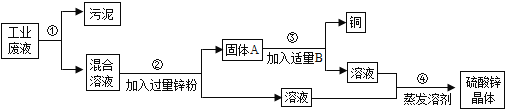
(1)步骤②中分离物质的方法是 。
(2)步骤②中发生反应的化学方程式为 ,基本类型为 反应。
(3)固体A的成分是 。
(4)步骤③中加入的B物质是 。
【答案】(1)过滤;(2)![]() ; 置换;(3)
; 置换;(3)![]() 、
、![]() ;(4)稀硫酸;
;(4)稀硫酸;
【解析】
试题分析:该反应的流程是将工业废液过滤得到污泥和硫酸锌与硫酸铜的混合液;向混合液中加入过量的锌,得到硫酸铜溶液及固体A,固体A的成分是过量的锌和生成的铜;向锌和铜的混合物中加适量的硫酸,得到铜和硫酸锌溶液;将两部分硫酸锌溶液蒸发溶剂得到硫酸锌晶体。
(1)分离固体和液体的方法是过滤;(2)②中的反应是锌和硫酸铜反应生成铜和硫酸锌;该反应是一种单质和一种化合物反应,生成另一种单质和另一种化合物,故是置换反应;(3)固体A的成分是锌和铜;(4)因为加入锌后得到的溶液是硫酸锌溶液,故将锌转化成硫酸锌可以向锌和铜的混合物中加入少量的硫酸;

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】今天是某校实验室开放日,晓明同学用锌和稀硫酸反应制取氢气。先向气体发生装置中加入一定量的锌粒,然后将60克稀硫酸分三次加入,每次生成气体的质量如下表:
次数 | 第一次 | 第二次 | 第三次 |
加入稀硫酸质量/g | 20 | 20 | 20 |
生成氢气的质量/g | 0.08 | 0.08 | 0.04 |
试计算:
(1)共制得氢气_____g和共加入_____g锌粒。
(2)实验所用稀硫酸中溶质的质量分数。_____(写出计算过程)
【题目】如图所示的密闭装置中,先将甲中液体滴入丙中,观察到气球明显鼓起,一段时间后气球恢复原状;再将乙中液体滴入丁中,气球又明显鼓起。下列组合正确的是

滴管甲 | 烧杯丙 | 滴管乙 | 烧杯丁 | |
① | 水 | 硝酸铵 | 稀硫酸 | 生铁 |
② | 水 | 浓硫酸 | 稀盐酸 | 草木灰 |
③ | 水 | 生石灰 | 食醋 | 镁条 |
A. ①②③B. ①②C. ①③D. ②③