题目内容
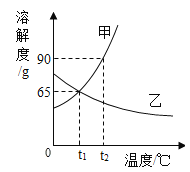
【题目】甲和乙两种物质的溶解度曲线如图所示。
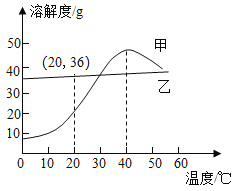
(1)请写出图像中(20,36)表达的含义_____________。
(2)在40℃时,若把甲的不饱和溶液变成饱和溶液,在保持溶质质量分数不变的情况下可采取的方法为________________、_________(两种方法)。
(3)在生产生活中,我们常常采取__________获得乙物质晶体。
(4)下列说法正确的是__________。
①甲的溶解度随温度的升高而增大
②40℃时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法
③20℃时,向125g溶质质量分数为20%的乙溶液中加入15g乙固体并振荡,有固体不溶解
④将相同质量的甲和乙的饱和溶液分别从40℃降温至10℃,甲析出晶体的质量多
【答案】乙在20℃时的溶解度为36 g 升温 降温 蒸发结晶 ②③④
【解析】
(1)根据溶解度曲线可知,图像中(20,36)表达的含义乙在20℃时的溶解度为36 g;
(2)在小于40℃时,甲的溶解度随温度的升高而降低,在大于40℃时,甲的溶解度随温度的升高而降低。在40℃时,若把甲的不饱和溶液变成饱和溶液,在保持溶质质量分数不变的情况下可采取的方法为升温、降低;
(3)乙的溶解度随温度的升高而升高,受温度影响不大,在生产生活中,我们常常采取蒸发结晶获得乙物质晶体;
(4)①在小于40℃时,甲的溶解度随温度的升高而降低,在大于40℃时,甲的溶解度随温度的升高而降低,故①错误;
②在小于40℃时,甲的溶解度随温度的升高而降低,在大于40℃时,甲的溶解度随温度的升高而降低,40℃时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法,故②正确;
③125g溶质质量分数为20%的乙溶液中乙的质量=125g×20%=25g,溶剂的质量=125g-25g=100g,乙在20℃时的溶解度为36 g,100g水中最多溶解36g,20℃时,向125g溶质质量分数为20%的乙溶液中加入15g乙固体并振荡,有固体不溶解,故③正确;
④小于40℃时,甲、乙的溶解度随温度的降低而降低,甲的溶解度受温度影响较乙大,将相同质量的甲和乙的饱和溶液分别从40℃降温至10℃,甲析出晶体的质量多,故正确。故选②③④。