题目内容
【题目】化学实验是学好化学的基础,某校学生进行了以下化学实验:
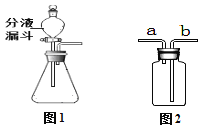
Ⅰ.甲小组利用下列几种发生装置和收集装置制取O2。请回答下列问题:
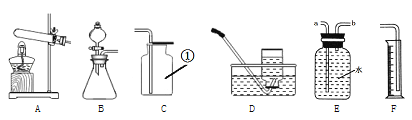
(1)写出标号①的仪器名称_______
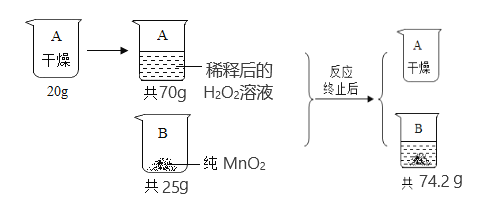
(2)实验室用双氧水和和二氧化锰制取并收集较纯的氧气时,选用的装置是________(填字母),二氧化锰的作用是________。写出该反应的化学方程式_________________________。
(3)将右侧E和F装置连接,可测量氧气体积,氧气应从_______(填“a”或b)口通入。
Ⅱ.乙小组的同学对一包在空气中敵口放置了一段时间的碱石灰的成分进行探究。
【提出问题】这包久置的碱石灰样品的成分是什么?
【查阅资料}】①碱石灰是由CaO和NaOH固体混合而成,通常用于吸收二氧化碳及干燥气体。②熟石灰固体溶解度小,溶于水放出的热量少,可以忽路不计。
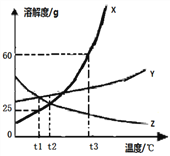
【提出猜想】该碱石灰的主要成分可能含有CaO、NaOH、 Na2CO3、 CaCO3和_______等五种物质。
【实验探究】小组的同学设计实验并进行验证,过程如下:
①小明取部分该碱石灰样品于试管中,加少量水后无放热现象,说明这包碱石灰样品中不含CaO和_______。继续加足量水,振荡,静置后有白色沉淀。
②从小明的试管中取上层清液于另一试管中,向其中滴加过量BaCl2溶液,有白色沉淀生成。
③把过程②所得物质过滤,向滤液中滴加无色酚酞溶液,溶液变成红色。
【思考分析】①上述实验步骤①中所得白色沉淀为_______。
②证明上述实验步骤②中加入的BaCl2溶液已过量的方法是___________________。
③若向上述实验步骤③中改滴紫色石蕊试液,观观察到的现象为 _______________。
【解释结论】该碱石灰样品中一定含有的物质是_____________________________。
【答案】 集气瓶 BD(或BE) 作催化剂 2H2O2![]() 2H2O+O2↑ b Ca(OH)2 NaOH CaCO3 继续往上层清液中滴加BaCl2,无沉淀产生,说明BaCl2已经过量(取上层清液少许于试管中,滴加Na2CO3溶液,有沉淀产生,说明BaCl2已过量) 溶液变蓝色 Na2CO3、Ca(OH)2
2H2O+O2↑ b Ca(OH)2 NaOH CaCO3 继续往上层清液中滴加BaCl2,无沉淀产生,说明BaCl2已经过量(取上层清液少许于试管中,滴加Na2CO3溶液,有沉淀产生,说明BaCl2已过量) 溶液变蓝色 Na2CO3、Ca(OH)2
【解析】(1)标号①的仪器名称集气瓶;(2)实验室用双氧水和和二氧化锰制取并收集较纯的氧气时,选用的发生装置是固液常温型B,氧气的密度比空气大可用向上排空气法收集,选择装置C,氧气难溶于水,可用排水法收集,选择装置D或E,其中排水法收集气体较纯;二氧化锰的作用是催化作用。该反应的化学方程式2H2O2 ![]() 2H2O+O2↑;(3)将右侧E和F装置连接,可测量氧气体积,氧气应从b口通入;Ⅱ. 【提出猜想】碱石灰是由CaO和NaOH固体混合而成,氧化钙和水反应生成氢氧化钙,氢氧化钙和空气中的二氧化碳反应生成碳酸钙沉淀和和水,氢氧化钠和二氧化碳反应生成碳酸钠和水,放置后,该碱石灰的主要成分可能含有CaO、NaOH、 Na2CO3、 CaCO3和Ca(OH)2等五种物质。【实验探究】①氢氧化钠溶于水放出大量热,氧化钙和水反应放出大量热。取部分该碱石灰样品于试管中,加少量水后无放热现象,说明这包碱石灰样品中不含CaO和氢氧化钠。②从小明的试管中取上层清液于另一试管中,向其中滴加过量BaCl2溶液,有白色沉淀生成,说明有碳酸钠,。③把过程②所得物质过滤,向滤液中滴加无色酚酞溶液,溶液变成红色,说明有氢氧化钠。【思考分析】①上述实验步骤①中所得白色沉淀为碳酸钙,因变质生成的碳酸钙是难溶于水的沉淀。②证明上述实验步骤②中加入的BaCl2溶液已过量的方法是继续往上层清液中滴加BaCl2,无沉淀产生,说明BaCl2已经过量(取上层清液少许于试管中,滴加Na2CO3溶液,有沉淀产生,说明BaCl2已过量) 。③碱性溶液能使紫色石蕊试液变蓝,若向上述实验步骤③中改滴紫色石蕊试液,观察到的现象为溶液变蓝色。【解释结论】该碱石灰样品中一定含有的物质是Na2CO3、Ca(OH)2。
2H2O+O2↑;(3)将右侧E和F装置连接,可测量氧气体积,氧气应从b口通入;Ⅱ. 【提出猜想】碱石灰是由CaO和NaOH固体混合而成,氧化钙和水反应生成氢氧化钙,氢氧化钙和空气中的二氧化碳反应生成碳酸钙沉淀和和水,氢氧化钠和二氧化碳反应生成碳酸钠和水,放置后,该碱石灰的主要成分可能含有CaO、NaOH、 Na2CO3、 CaCO3和Ca(OH)2等五种物质。【实验探究】①氢氧化钠溶于水放出大量热,氧化钙和水反应放出大量热。取部分该碱石灰样品于试管中,加少量水后无放热现象,说明这包碱石灰样品中不含CaO和氢氧化钠。②从小明的试管中取上层清液于另一试管中,向其中滴加过量BaCl2溶液,有白色沉淀生成,说明有碳酸钠,。③把过程②所得物质过滤,向滤液中滴加无色酚酞溶液,溶液变成红色,说明有氢氧化钠。【思考分析】①上述实验步骤①中所得白色沉淀为碳酸钙,因变质生成的碳酸钙是难溶于水的沉淀。②证明上述实验步骤②中加入的BaCl2溶液已过量的方法是继续往上层清液中滴加BaCl2,无沉淀产生,说明BaCl2已经过量(取上层清液少许于试管中,滴加Na2CO3溶液,有沉淀产生,说明BaCl2已过量) 。③碱性溶液能使紫色石蕊试液变蓝,若向上述实验步骤③中改滴紫色石蕊试液,观察到的现象为溶液变蓝色。【解释结论】该碱石灰样品中一定含有的物质是Na2CO3、Ca(OH)2。

【题目】下表是日常生活中常用各种清洗剂。
名称 | 洗涤灵 | 洁厕灵 | 炉具清洁剂 | 活氧彩漂 |
产品样式 |
|
|
|
|
有效成分或功能 | 清洗油污 | 盐酸 | 氢氧化钠 | 过氧化氢 |
(1)使用洗涤灵清洗餐具上的油污,这是因为它具有_____功能。
(2)清除以下物质,可使用洁厕灵的是_______(填字母序号)。
A.铁锈 B.油污 C.水垢 D.木炭还原氧化铜后,试管内壁残余的红色痕迹
(3)将洁厕灵滴入炉具清洁剂中,如图甲所示、
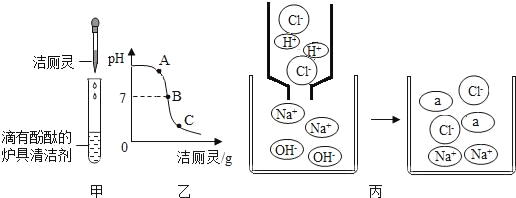
①甲中发生反应的化学方程式为______________
②若反应后溶液呈红色,则反应后溶液中的溶质是(酚酞除外)__________,此时溶液可用图乙中_____(选填A、B、C)点处表示。
③丙中反应没有明显现象,为证明反应发生,可加入的试剂有________。
A.无色酚酞溶液 B.硝酸钾溶液 C.硝酸银溶液 D.锌粒