题目内容
【题目】下列各组物质充分反应后,溶液质量随时间变化符合如图的是( )
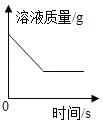
A.铁片浸入稀硫酸中
B.铁片浸入硫酸铜溶液中
C.氧化铁粉末加入稀盐酸中
D.碳酸氢钠粉末加入稀盐酸中
【答案】B
【解析】
A、根据铁和硫酸反应生成硫酸亚铁和氢气进行分析;
B、根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
C、根据氧化铁和盐酸反应生成氯化铁和水进行分析;
D、根据碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳进行分析。
A、每56份质量的铁和盐酸反应生成2份质量的氢气,溶液质量逐渐增大,然后不变,故A错误;
B、每56份质量的铁和硫酸铜反应生成64份质量的铜,溶液质量逐渐减小,然后不变,故B正确;
C、氧化铁和盐酸反应生成氯化铁和水,溶液质量逐渐增大,故C错误;
D、每84份质量的碳酸氢钠和盐酸反应生成44份质量的二氧化碳,溶液质量逐渐增大,故D错误。
故选:B。

 阅读快车系列答案
阅读快车系列答案【题目】某物质在点燃的条件下发生反应,生成物和反应物共四种,它们的微观示意图和反应前后的质量如下表所示。
物质序号 | 甲 | 乙 | 丙 | 丁 |
|
微观示意图 |
|
|
|
| |
反应前质量/g | 68 | 100 | 1 | 0 | |
反应后质量/g | 0 | x | y | z |
(1)由![]() 构成的物质中
构成的物质中![]() 所代表的元素的化合价为______;
所代表的元素的化合价为______;
(2)表中的四种物质中,属于氧化物的是______ (填化学式);
(3)上述反应的化学方程式为______;
(4)一位同学在计算x、y和z数值的过程中,列出了以下等式,其中正确的是______(填字母序号)。
A.x + y +x = 169 B.y + z = 168 C.(100-x):z = 32:64 D.(l00-x):(y-1) = 8:3
【题目】小丽来到实验室,看到实验桌上有一瓶敞口放置的氢氧化钠固体,于是她对这瓶氢氧化钠固体的成分展开探究。
[提出问题]这瓶氢氧化钠固体是否变质?
[猜想假设]猜想一:没有变质,固体物质是NaOH;
猜想二:部份变质,固体物质是NaOH和Na2CO3;
猜想三:完全变质,固体物质是_____。
[实验探究]为了探究固体成分,他们分别进行了如下实验:
(1)写出氢氧化钠变质的化学方程式_____。
(2)为了进一步确定这瓶固体的成分,丙同学设计了如下方案,请你完成下列实验报告:
实验方案 | 实验步骤 | 实验的现象 | 实验结论 |
实验方案Ⅰ | 取样于试管中 ,加入过量稀盐酸。 | 出现大量气泡 | 说明猜想一不成立 |
实验方案Ⅱ | ①取样于试管中,加水溶解,滴入酚酞溶液 | 溶液变红色 | 说明猜想二成立 |
②向①反应后溶液,滴入过量的Ca(OH)2溶液 | 产生白色沉淀,溶液显_____色 | ||
实验方案Ⅲ | ①取样于试管中,加水溶解,滴入酚酞溶液 | 溶液变红色 | 说明猜想三成立。 |
②向①反应后溶液,滴入过量的CaCl2溶液 | 产生_____,溶液由红色变成无色 |
[反思和评价]
1、在设计的实验方案中,其中有一种不合理的方案是_____。
2、在实验方案Ⅲ的探究中,能代替CaCl2溶液进行实验的是_____。 (填序号)
①稀硝酸;②Ba(OH)2溶液:③Ba(NO3)2溶液;④K2CO3溶液: ⑤Ca(NO3)2 溶液
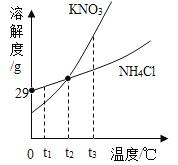
【题目】如表列出了KNO3与NaCl在不同温度时的溶解度:
温度(℃) | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
KNO3溶解度(g) | 13.3 | 20.9 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl溶解度(g) | 35.7 | 35.8 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
现有含123g KNO3与17.9g NaCl的混合物,某同学设计了以下实验除去KNO3中的NaCl。
①向混合物中加入适量水,加热溶解;
②继续加热溶液至100℃并恒温蒸发浓缩成硝酸钾的热饱和溶液;
③将溶液降温至10℃,仅得到KNO3晶体,过滤,将所得KNO3晶体洗涤并干燥。
(1)在步骤②中,为确保没有晶体析出,溶液中至少要保留_____g水
(2)在步骤③中,最多可得到KNO3晶体_____g
(3)除去KNO3中少量NaCl的主要实验流程可用如图表示:
![]()
方框中缺少的步骤是_____;
(4)洗涤时,应选用少量_____(选填“热水”或“冷水”);证明已经洗涤干净的方法是_____。