题目内容
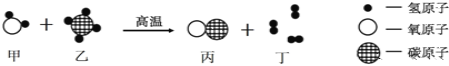
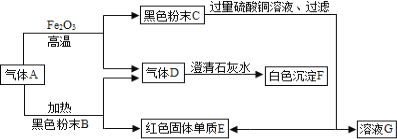
【题目】根据下列化合物与单质相互转化的关系回答:
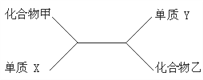
(1)若乙的溶液是浅绿色,Y是红色固体,则X是___,如:(用化学方程式表达)____
(2)在常温下若乙是气体,则X是________,如:(用化学方程式表达)__________
(3)在常温下若甲是固体,乙是无色液体,则X是________,如:(用化学方程式表达)_______
【答案】 Fe Fe+CuSO4===Cu+FeSO4 C C+2CuO![]() 2Cu+CO2↑ H2 H2+CuO
2Cu+CO2↑ H2 H2+CuO![]() Cu+H2O
Cu+H2O
【解析】(1)亚铁离子在溶液中显浅绿色,题中描述的现象为铁置换铜盐中的铜的反应现象,故X是Fe,比如铁与硫酸铜反应生成铜和硫酸亚铁,反应方程式为:Fe+CuSO4===Cu+FeSO4;
(2)在常温下若乙是气体,X、Y是单质,则反应可能是碳还原氧化铜的反应,故X是C;反应方程式为:C+2CuO![]() 2Cu+CO2↑;
2Cu+CO2↑;
(3)在常温下若甲是固体,乙是无色液体,无色液体最常见的是水,故X是H2;甲是氧化铜,氢气与氧化铜在高温的条件下反应生成铜和水,反应方程式为:H2+CuO![]() Cu+H2O;
Cu+H2O;

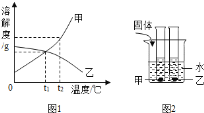
【题目】下表是NaCl、KNO3在不同温度时的溶解度:
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
据此数据,判断下列说法错误的是
A. KNO3和NaCl的溶解度曲线在20℃—30℃温度范围内会相交
B. 在60℃时,KNO3的饱和溶液105g加入95g水后,溶液中溶质的质量分数为27.5%
C. 在20℃时,NaCl和KNO3固体各35g分别加入两只各盛有100g水的烧杯中,均不能形成饱和溶液
D. 从含有少量NaCl的KNO3饱和溶液中得到较多的KNO3晶体,通常可采用冷却热饱和溶液的方法