题目内容
【题目】下列排列顺序正确的是
A. 地壳中元素的含量![]() B. 硫元素的化合价
B. 硫元素的化合价![]() C. 空气中物质的含量
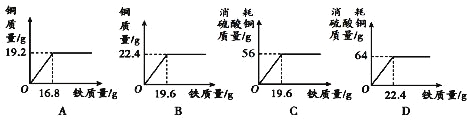
C. 空气中物质的含量![]() D. 铁元素的质量分数
D. 铁元素的质量分数![]()
【答案】B
【解析】A、地壳中元素含量由多到少顺序是:氧、硅、铁,错误;
B、根据在化合物中正负化合价代数和为零,硫元素在SO2;S;H2S;中的化合价分别是
x+(-2)×2=0,0,y+(+1)×2=0,可得x=+4,0,y=-2,正确;C、空气中物质含量由高到低的顺序是氮气、氧气、二氧化碳,错误;D、因为S元素的相对原子质量是32,数值相当于2个O原子的相对原子质量;可以将S看成是两个氧原子;观察四种物质的化学式可知:FeO中一个铁原子对应1个氧原子,Fe2O3中一个铁原子对应3/2个氧原子,FeS中一个铁原子对应2个氧原子;则氧原子数越大的铁元素的质量分数就越小;铁元素质量分数由高到低排列:FeO>Fe2O3>FeS错误。故选B。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案【题目】过碳酸钠(化学式为2Na2CO33H2O2)俗名固体双氧水。溶于水可看作是Na2CO3溶液和H2O2溶液混合。为了方便保存,过碳酸钠样品可能添加少量的MgSO4和硅酸镁中的一种或二种作为稳定剂。已知①双氧水可用于供氧、消毒和漂白;②硅酸镁不溶于水。
(1)过碳酸钠的用途不合理的是 。
A.鱼池供氧剂 B.消毒剂 C.干燥剂 D.漂白剂
(2)取少量过碳酸钠样品于烧杯中,加入足量蒸馏水,有不溶于水的固体产生。判断样品中 有硅酸镁。(填写“可能”或“一定”)
(3)利用实验室限选试剂,设计实验确定该样品中是否添加少量的MgSO4。
限选试剂:稀盐酸、稀H2SO4、BaCl2溶液、蒸馏水、AgN03溶液
实验操作 | 预期现象和必要结论 |
步骤:1:取少量样品于烧杯中,缓慢加入足量蒸馏水,充分搅拌,静置,过滤。 |
|
步骤2:取少量步骤1所得的滤液于试管中,加入 ,振荡后静置。 | |
步骤3:取少量步骤2所得的溶液于试管中, 。 | ,说明样品中有MgSO4。 ,说明样品中没有MgSO4。 |