题目内容
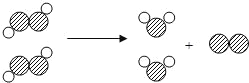
【题目】图中A~M是初中化学常见的物质,且分别由H、C、O、Na、S、Cl、K、Fe中一种或几种元素组成。B、C、E、F、M均由两种元素组成,B为铁锈的主要成分,D属于盐,固态E叫做“干冰”;A、D、H均由三种元素组成,H在实验室可用于制取氧气;G是焙制糕点所用的发酵粉的主要成分之一。图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
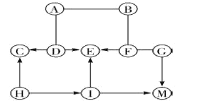
(1)写出化学式:G_______,B______,E______。
(2)写出H→I反应的化学方程式______________________________________。
(3)写出A与D反应的化学方程式__________________________。
【答案】NaHCO3 Fe2O3 CO2 2KClO3![]() 2KCl+3O2↑ K2CO3+H2SO4═K2SO4+H2O+CO2↑
2KCl+3O2↑ K2CO3+H2SO4═K2SO4+H2O+CO2↑
【解析】
B为铁锈的主要成分,故B是氧化铁,固态E叫做“干冰”,故E是二氧化碳;H由三种元素组成,H在实验室可用于制取氧气,故H是氯酸钾;G是焙制糕点所用的发酵粉的主要成分之一,故G是碳酸氢钠;氧化铁能与由三种元素组成的A反应,故A是硫酸,能与由两种元素组成的F反应,F还能生成二氧化碳,与碳酸氢钠反应,故F是盐酸,氯酸钾能生成C,生成的I能生成二氧化碳,故I是氧气,氧气和碳酸氢钠都能生成M,故M是水;C是氯化钾,D能生成氯化钾,故D是碳酸钾,带入框图,推断合理;
(1)G是碳酸氢钠,B是氧化铁,E是二氧化碳,故填:NaHCO3;Fe2O3;CO2;
(2)氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,故填:2KClO3![]() 2KCl+3O2↑;
2KCl+3O2↑;
(3)A是硫酸,D是碳酸钾,二者反应生成硫酸钾、水和二氧化碳,故填:K2CO3+H2SO4═K2SO4+H2O+CO2↑。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注.某化学兴趣小组对Mg、Ti、Ag的金属活动性顺序进行探究.
[提出假设]A.Ti>Mg>Ag; B.Mg>Ag>Ti; C._____.
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速度越快,则该金属活动性越强.
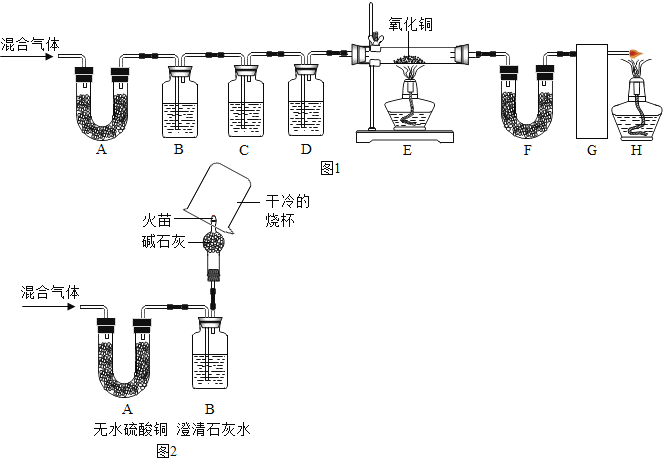
[实验设计]同温下,取大小相同的这三种金属薄片,分别投入等体积、等质量分数的足量稀盐酸中,观察现象.请填空:
(1)三种金属加入盐酸前都先用砂纸将表面擦光亮,其目的是_____.
(2)根据下表中的实验现象填空:
Ti | Mg | Ag | |
实验现象 | 产生气泡速度缓慢 | 产生气泡速度快 | 无任何现象 |
[结论]假设_____正确(填“A”或“B”或“C”)
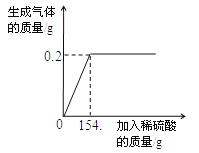
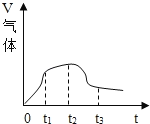
(3)在做镁条与稀盐酸反应过程中观察到产生气体体积与反应时间有如图所示关系:
则t1~t2时间内反应速率逐渐加快的主要原因是_____. t2~t3时间内反应速率逐渐减慢的原因是_____.
(4)在[实验设计]中,如果所用盐酸的溶质质量分数不同,是否一定能够得出正确结论?_____(填“是”或“否”),理由是_____.
(5)你是否还知道其他方法来比较这三种金属的活动性(可供选择的药品:Ti、Mg、Ag、TiCl2溶液、MgCl2溶液、AgNO3溶液).
①_____;②_____.
【题目】已知20℃时,NaCl和NaNO3的溶解度分别为36g和88g.
| 序号 | ① | ② | ③ | ④ | ⑤ |
固体种类 | NaCl | NaCl | NaNO3 | NaNO3 | NaNO3 | |
固体的质量/g | 30 | 60 | 30 | 60 | 90 | |
水的质量/g | 100 | 100 | 100 | 100 | 100 |
下列关于①-⑤实验操作所得溶液说法不正确的是
A. 溶质质量:①<②B. 溶液质量:②<④C. 溶质质量分数:①=③D. ⑤中溶液质量:190g