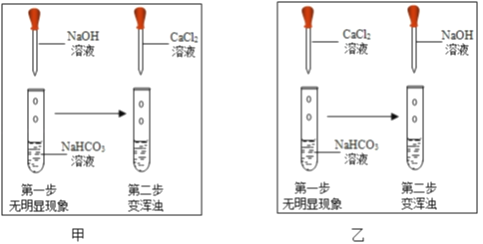
题目内容
【题目】有一包白色固体样品,可能是碳酸钠、硫酸钡、氢氧化钠、氯化钙中的一种或几种,小菁设计如下实验来探究其成分,下列判断不正确的
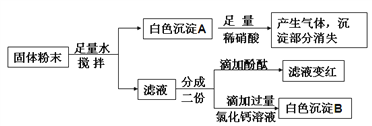
A. 原固体中一定有硫酸钡、碳酸钠和氯化钙 B. 滤液中只含有一种阳离子Na+
C. 原固体中一定有氢氧化钠 D. 探究过程中的发生的反应都属于复分解反应
【答案】C
【解析】根据碳酸钠能和氯化钙反应生成白色的碳酸钙沉淀,碳酸钙能与酸反应生成气体;硫酸钡不溶于水且不溶于酸的白色沉淀;而碳酸钠溶液也为碱性;故:A、原固体中一定有硫酸钡、碳酸钠和氯化钙,正确;B、滤液中只含有一种阳离子Na+,正确;C、因为碳酸钠溶液也为碱性,故原固体中不一定有氢氧化钠,错误;D、因为碳酸钠能和氯化钙反应生成白色的碳酸钙沉淀,碳酸钙能与酸反应生成气体,都为复分解反应,故探究过程中的发生的反应都属于复分解反应,正确。故选C。

练习册系列答案
相关题目