题目内容
【题目】下列为实验室常用的实验装置,回答问题:
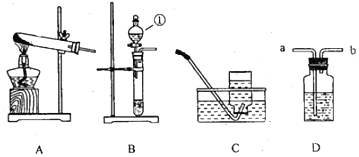
![]() 写出图中标号仪器的名称:
写出图中标号仪器的名称:![]() ______。
______。
![]() 若该实验选择装置A、C来制取氧气,何时收集氧气最好:______;请写出该反应的化学方程式______;该反应属于四种基本反应类型中的______反应。
若该实验选择装置A、C来制取氧气,何时收集氧气最好:______;请写出该反应的化学方程式______;该反应属于四种基本反应类型中的______反应。
![]() 某同学在实验室从图中选用适当的发生装置成功的制备了
某同学在实验室从图中选用适当的发生装置成功的制备了![]() 该反应的化学方程式是______,为了进一步验证产生的
该反应的化学方程式是______,为了进一步验证产生的![]() 化学性质,该同学将气体通入图D装置中
化学性质,该同学将气体通入图D装置中![]() 装有紫色石蕊溶液
装有紫色石蕊溶液![]() ,气体从______
,气体从______![]() 填“a”或“b”
填“a”或“b”![]() 端通入后溶液变红了,变红的原因是
端通入后溶液变红了,变红的原因是![]() 用化学方程式表示
用化学方程式表示![]() ______。
______。
【答案】分液漏斗 气泡连续均匀冒出时 ![]() 分解
分解 ![]() a
a ![]()
【解析】
![]() 通过分析题中所指仪器的名称和作用可知,
通过分析题中所指仪器的名称和作用可知,![]() 是分液漏斗;
是分液漏斗;
![]() 排水法收集氧气的正确时刻是:气泡连续均匀冒出时,反应物是固体,反应条件是加热,试管口没有放棉花,所以该反应是氯酸钾制取氧气,氯酸钾在二氧化锰的催化作用下分解生成氯化钾和氧气,化学方程式为:
排水法收集氧气的正确时刻是:气泡连续均匀冒出时,反应物是固体,反应条件是加热,试管口没有放棉花,所以该反应是氯酸钾制取氧气,氯酸钾在二氧化锰的催化作用下分解生成氯化钾和氧气,化学方程式为:![]() ,该反应属于分解反应;
,该反应属于分解反应;
![]() 碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:
碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:![]() ,二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊变红色,所以气体从a端通入后溶液变红了,变红的原因是:
,二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊变红色,所以气体从a端通入后溶液变红了,变红的原因是:![]() 。
。
故答案为:![]() 分液漏斗;
分液漏斗;
![]() 气泡连续均匀冒出时,
气泡连续均匀冒出时,![]() ,分解;
,分解;
![]() ,a,
,a,![]() 。
。
![]() 根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
![]() 根据排水法收集氧气的正确时刻是:气泡连续均匀冒出时,反应物是固体,反应条件是加热,试管口没有放棉花,所以该反应是氯酸钾制取氧气,氯酸钾在二氧化锰的催化作用下分解生成氯化钾和氧气进行分析;
根据排水法收集氧气的正确时刻是:气泡连续均匀冒出时,反应物是固体,反应条件是加热,试管口没有放棉花,所以该反应是氯酸钾制取氧气,氯酸钾在二氧化锰的催化作用下分解生成氯化钾和氧气进行分析;
![]() 根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊变红色进行分析。
根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊变红色进行分析。

 孟建平名校考卷系列答案
孟建平名校考卷系列答案【题目】某化学探究小组用盐酸与大理石的反应来研究影响反应速率的因素。实验温度为![]() 、
、![]() ;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙
;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙![]() 的大理石10g;所用盐酸的质量分数为
的大理石10g;所用盐酸的质量分数为![]() 、
、![]() ,每次实验盐酸的用量为
,每次实验盐酸的用量为![]() 假设
假设![]() 、
、![]() 的盐酸的密度均为
的盐酸的密度均为![]() ;大理石中杂质不与盐酸反应
;大理石中杂质不与盐酸反应![]() 。
。
(提岀假设)盐酸与大理石反应的反应速率与所用盐酸的质量分数、大理石规格、反应温度有关。
![]() (实验设计与实施)完成以下实验设计方案并实验
(实验设计与实施)完成以下实验设计方案并实验
实验 编号 |
| 大理石 规格 | 盐酸的 质量分数 | 完全反应 的时间 | 实验目的 |
| 25 | 粗颗粒 |
| 160 |
|
| ______ | ______ | ______ | 210 | |
| 35 | 粗颗粒 |
| 60 | |
| ______ | ______ | ______ | 100 |
![]() 从实验
从实验![]() 和
和![]() 可以得出的实验结论是:______。
可以得出的实验结论是:______。
![]() 含碳酸钙
含碳酸钙![]() 的大理石中,含有碳酸钙的质量为______g。
的大理石中,含有碳酸钙的质量为______g。
![]() 碳酸钙与盐酸反应的化学方程式为______;若
碳酸钙与盐酸反应的化学方程式为______;若![]() 中的大理石与过量稀盐酸充分反应,能生成二氧化碳的质量为______
中的大理石与过量稀盐酸充分反应,能生成二氧化碳的质量为______![]() 只列计算式,已知碳酸钙的相对分子质量为100,二氧化碳的相对分子质量为
只列计算式,已知碳酸钙的相对分子质量为100,二氧化碳的相对分子质量为![]() 。
。
【题目】下列实验方法一定能达到实验目的是![]()
![]()
选项 | 实验目的 | 实验方法 |
A | 检验一瓶气体是否为 | 将燃着的木条伸入瓶中 |
B | 鉴别 | 分别点燃,在火焰上方罩一干冷烧杯 |
C | 除去 | 通过灼热的CuO |
D | 除去KCl中的少量 | 加入 |
A. A B. B C. C D. D