题目内容
【题目】将氯化钠和氯化铜的固体混合物20g完全溶于100g水中,再向所得的溶液中加入溶质质量分数为10%的NaOH溶液。有关的变化如图所示。(反应的化学方程式为:CuCl2+2NaOH=Cu(OH)2↓+2NaCl)请计算:

(1)NaOH中氧元素和氢元素的质量比为______________。
(2)求恰好完全反应时,所用NaOH溶液的质量。(写出计算过程)
(3)求恰好完全反应时溶液中溶质的质量分数。(写出计算过程,结果精确到0.1%)
【答案】(1)16:1 (2)40g (3)12.3%
【解析】
(1)NaOH中氧元素和氢元素的质量比为16:1。
(2)解:设CuCl2的质量为x,恰好完全反应时所用NaOH的质量为y,生成NaCl的质量为z。
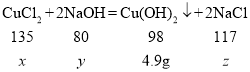
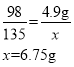

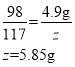
恰好完全反应时,所用NaOH溶液的质量:![]() 。
。
(3)恰好完全反应时溶液中溶质的质量分数:![]()
答:恰好完全反应时消耗NaOH的质量为40g;恰好完全反应时溶液中溶质的质量分数为12.3%。

练习册系列答案
相关题目
【题目】黄铜是一种重要的金属,它是铜和锌的合金,可用来制造机器、电器零件及日常用品。为了测定黄铜样品的组成,取五份样品分别加稀硫酸反应,其实验数据记录如下:
样品 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 |
取样品质量(g) | 40.0 | 40.0 | 40.0 | 40.0 | 40.0 |
取稀硫酸质量(g) | 30.0 | 60.0 | 90.0 | 120.0 | 150.0 |
产生气体质量(g) | 0.3 | 0.6 | 0.9 | 1.0 | 1.0 |
按要求回答下列问题:
(1)根据实验数据分析,从第________份开始,金属已经反应完全了。
(2)列式计算该黄铜样品中金属锌的质量分数。(要求写出计算过程)