题目内容
【题目】下图所示为实验室常见气体制备、净化、干燥和收集的部分仪器。
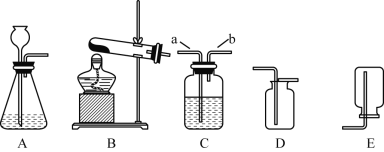
(1)某同学打算用高锰酸钾制取并收集干燥的气体,则可选择上述装置中_____(填字母序号),写出该反应的化学方程式_____。
(2)若打算制取二氧化碳,则发生装置应选择_____(填字母序号),在C装置中装入浓硫酸来干燥制取的气体,则应该从_____(填“a”或者“b”)端通入气体。
(3)用上述制取二氧化碳实验后的残留液进行pH检测、过滤、蒸发的操作训练。
①对固体残留物进行过滤,除了需要玻璃棒和烧杯外,还需要的玻璃仪器是_____;
②用pH试纸检测滤液的酸碱度,检测pH的操作方法是:把一片pH试纸置于干燥洁净的表面皿上,_____;测得溶液pH=4,说明有_____剩余。
③取上述少量滤液进行蒸发,蒸发过程玻璃棒不断搅拌的作用是_____。
【答案】BD ![]() A a 漏斗 用玻璃棒蘸取滤液点于pH试纸上待颜色变化稳定后用标准比色卡比对得出pH数值 盐酸 防止局部温度过高,导致液滴飞溅
A a 漏斗 用玻璃棒蘸取滤液点于pH试纸上待颜色变化稳定后用标准比色卡比对得出pH数值 盐酸 防止局部温度过高,导致液滴飞溅
【解析】
(1)某同学打算用高锰酸钾制取并收集干燥的气体,则可选择固体加热装置B;氧气的密度大于空气,应该用向上排空气法收集,选择装置D;高锰酸钾加热产生锰酸钾、二氧化锰和氧气的化学方程式![]() 。
。
(2)若打算制取二氧化碳,则应选择固液发生装置(不需要加热)A,在C装置中装入浓硫酸来干燥制取的气体,则应该“长管进、短管出”从a端通入气体进行干燥。
(3)①对固体残留物进行过滤,除了需要玻璃棒和烧杯外,还需要的玻璃仪器是漏斗(带滤纸,用于过滤);
②用pH试纸检测滤液的酸碱度,检测pH的操作方法是:把一片pH试纸置于干燥洁净的表面皿上,用玻璃棒蘸取滤液点于pH试纸上待颜色变化稳定后用标准比色卡比对得出pH数值;测得溶液pH=4,说明混合溶液显酸性,有盐酸剩余。
③取上述少量滤液进行蒸发,蒸发过程玻璃棒不断搅拌的作用是:防止局部温度过高,导致液滴飞溅。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列实验方案不能达到实验目的是( )
序号 | A | B | C | D |
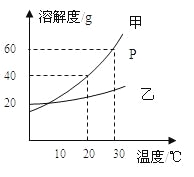
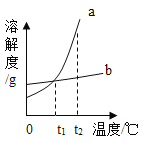
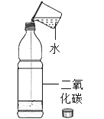
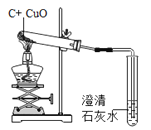
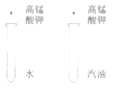
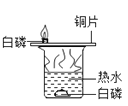
目的 | 证明二氧化碳溶于水且能和水反应 | 证明碳与氧化铜能发生反应 | 探究同种溶质在不同的溶剂的溶解性 | 探究燃烧的条件是燃烧需要氧气 |
方案 |
|
|
|
|
A. AB. BC. CD. D
【题目】废铁屑主要成分是铁,还有少量铁锈(Fe2O3),硫酸亚铁的生产工艺如图所示。

(1)在反应器中除发生Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,Fe2(SO4)3+Fe═3FeSO4这两个反应外,还会发生另外一个反应,化学方程式为:_____,反应器要加强通风,严禁烟火,其原因是:_____。
(2)将成品在有氧条件下焙烧,可转化为Fe2O3、SO2和SO3.为了提高SO3的产率,某实验小组进行了系列探究,实验数据如下:
编号 | 空气通入量/Ls﹣1 | 温度/℃ | SO2产率% | SO3产率/% |
a | 0.02 | 850 | 45.4 | 54.6 |
b | 0.06 | 850 | 30.5 | 69.5 |
c | 0.10 | 810 | 11.1 | 88.9 |
d | 0.10 | 850 | 11.1 | 88.9 |
e | 0.10 | 890 | 11.2 | 88.8 |
①本实验主要研究了哪些因素对SO3产率的影响_____。
②根据上表数据,生产过程中采用实验_____(填编号)的提取条件最合理。