题目内容
【题目】某工厂排出的废水中含有硝酸银,为了回收废水中的贵金属银,工厂进行了如下的操作。
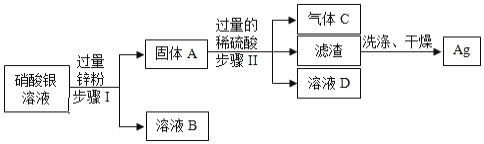
(1)锌的金属活动性比银的金属活动性______(选填“强”或者“弱”),固体 A 的成分有______。
(2)步骤 I、Ⅱ的名称是______,该操作中需要用到的玻璃仪器有烧杯、漏斗和______。
(3)若往溶液D中加入适量的氧化锌,可得到只含有一种溶质的溶液,则发生反应的化学方程式为______。
【答案】强 银、锌 过滤 玻璃棒 ZnO+H2SO4═ZnSO4+H2O
【解析】
硝酸银和锌反应生成硝酸锌和银,稀硫酸和锌反应生成硫酸锌和氢气,和氧化锌反应生成硫酸锌和水。
(1)锌的金属活动性比银的金属活动性强,硝酸银和锌反应生成硝酸锌和银,固体A的成分有反应生成的银和过量的锌。
(2)步骤I、Ⅱ是将固体和液体分离,故名称是过滤,该操作中需要用到的玻璃仪器有烧杯、漏斗和玻璃棒。
(3)若往溶液D中加入适量的氧化锌,氧化锌和稀硫酸反应生成硫酸锌和水,可得到只含有一种溶质硫酸锌的溶液,故发生反应的化学方程式为ZnO+H2SO4═ZnSO4+H2O。

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目