题目内容
我市锰矿资源丰富,MnO2是一种无机功能材料,主要用于制造干电池。当地某工厂加工得到了粗MnO2(主要含有杂质MnCO3,其它杂质忽略不计),为了测定其中MnO2的含量,称取57.5g粗MnO2样品,加入足量的稀硫酸溶液,产生CO2气体4.4g。
(已知:MnCO3+ H2SO4  MnSO4+H2O+CO2↑)
MnSO4+H2O+CO2↑)
试完成下列问题:(1)计算57.5g粗MnO2中含有MnCO3的质量,
(2)计算粗MnO2中的MnO2的质量分数。
(1) 11.5g (2)80%
解析试题分析:已知二氧化碳的质量,利用化学方程式根据反应的质量比可求出MnCO3的质量。
解 :(1)设57.5g粗MnO2中含有MnCO3的质量为x
MnCO3+ H2SO4  MnSO4+H2O+CO2↑
MnSO4+H2O+CO2↑
115 44
X 4.4g
115 /44 =x/4.4g
x=11.5g
MnO2的质量为:57.5g-11.5g=46.0g
粗MnO2中的MnO2的质量分数为: 46.0g /57.5g ×100%=80%
答:略
考点:利用化学方程式的计算

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案CO2和CO的混合气体3.6g与足量灼热的氧化铁充分反应后,将生成的气体全部通入80克质量分数为20%的氢氧化钠溶液中充分吸收,测得最终所得溶液的质量为84.4克,则原混合气体中CO质量为( )
| A.4.4g | B.2.8g | C. 1.4g | D.0.8g |
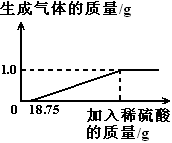
实验室用氯酸钾和二氧化锰制取氧气,加热一段时间后剩余固体混合物10g,继续加热至完全反应后(固体质量不再变化时)固体变为9.04g,再将固体加水充分溶解、过滤、干燥得到1.59g黑色固体。求10g剩余固体混合物中氯元素的质量分数为
| A.7.1% | B.35.5% | C.28.4% | D.42.6% |
某兴趣小组同学在一次实验中偶然发现:向盛有一定量铁粉的烧杯中加入稀硫酸有气泡产生,迅速加入一定量的氧化铜,搅拌,不再产生气泡、黑色粉末中逐渐出现红色固体后又有气泡产生。请回答:
① 若实验过程中共收集到0.1 g氢气,求生成0.1 g氢气所消耗的硫酸的物质的量。
② 加入氧化铜后,不产生气泡的原因是 (11) (用化学方程式表示)。
③ 充分反应后过滤,为确定滤液中的溶质成分,在滤液样品中插入一根铁丝,可能出现的现象和结论如下。
| 现象 | 结论 |
| (12) | 滤液中的溶质是FeSO4 |
| 有红色固体析出 | 滤液中的溶质可能有哪几种情况? (13) |
| (14) | 滤液中的溶质是 (15) |
一种石灰石样品的成分是CaCO3和SiO2。为了测定该样品中CaCO3的质量分数,现将100g盐酸等分5次加到35g此样品中,得到部分数据与图像。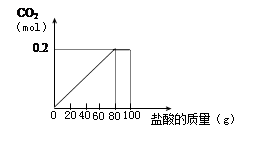
| 次数 | 第1次 | 第3次 | 第4次 |
| 加入盐酸的质量(g) | 20 | 20 | 20 |
| 剩余固体的质量(g) | 30 | a | 15 |
(1)石灰石样品中CaCO3的质量分数是 。
(2)第3次加入盐酸后,a为 g。
(3)反应共产生0.2mol CO2求加入盐酸溶质的质量分数。(根据化学方程式列式计算)
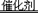 2CO2+N2,当有2.8gCO被转化时,计算同时被转化的NO的质量。
2CO2+N2,当有2.8gCO被转化时,计算同时被转化的NO的质量。