题目内容
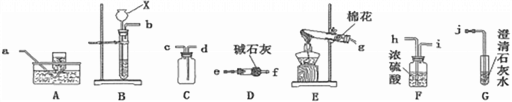
【题目】被称为“生命之源”的水(H2O)和被称为“绿色氧化剂”的双氧水(H2O2),通常情况下均为无色液体。在化学实验开放日,实验小组的同学用下面的方法鉴别水和双氧水两瓶无色液体,请填写有关内容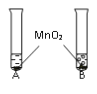
(1)B试管中发生反应的化学方程式:________________________。
(2)如何验证B试管中产生的气体(写出操作步骤、实验现象和结论)?______________________。
实验步骤 | 实验现象 | 实验结论 |
①将等体积的两种无色液体分别加入A、B两个试管中。 ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象。 | A试管中无明显现象 B试管中有气泡产生 | A试管中的无色液体是: _______________; B试管中的无色液体是:________; |
【答案】 水 双氧水 2H2O2![]() 2H2O+O2↑ 带火星的木条放在试管口,木条复燃证明产生的气体是氧气
2H2O+O2↑ 带火星的木条放在试管口,木条复燃证明产生的气体是氧气
【解析】本题考查了常温下过氧化氢分解生成水和氧气的检验方法。
(1)实验在常温下进行,常温下过氧化氢在二氧化锰催化下可以迅速分解出氧气,而水不能发生分解。加入二氧化锰后,无现象的为水,有气泡产生的液体为过氧化氢溶液。因此:
实验步骤 | 实验现象 | 实验结论 |
①将等体积的两种无色液体分别加入A、B两个试管中。 ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象。 | A试管中无明显现象 B试管中有气泡产生 | A试管中的无色液体是:水(H2O); B试管中的无色液体是:双氧水(H2O2); |
(1)双氧水分解时生成了水和氧气。反应的化学方程式是:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)氧气具有助燃性,能使带火星的木条复燃。验证氧气的方法是:带火星的木条放在试管口,木条复燃证明产生的气体是氧气。

【题目】小明在实验室发现一瓶氢氧化钠固体没有塞上瓶塞,于是他和他的同学一起对这瓶氢氧化钠固体展开探究,请你与他们一起进行探究。
【提出问题】这瓶氢氧化钠固体是否变质?
【猜想与假设】:①该氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠全部变质。
【查阅资料】CaCl2溶液呈中性。
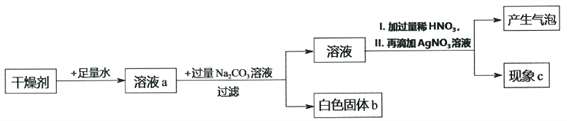
【设计实验】取该氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
实验步骤 | 实验现象 | 结论及解释 |
(1)取少量溶液A于试管中,向其中滴加足量的稀盐酸; | ___________ | 猜想①不成立 |
(2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液; | ____________ | 反应的化学方程式为: ______________ |
(3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液。 | 溶液呈红色 | 猜想 ________ 成立 |
【反思与交流】
(4)久置的氢氧化钠变质的原因是(用化学方程式表示) ___________________ 。
【探索与拓展】为进一步探究氢氧化钠的变质程度,小明称取18.6 g氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸100 g,反应后称得烧杯中溶液的质量为114.2 g。
(5)求该样品中碳酸钠的质量(要写出计算过程)。____________。
(6)该氢氧化钠的变质程度(即变质的氢氧化钠占变质前的氢氧化钠的质量分数)为______ 。