题目内容
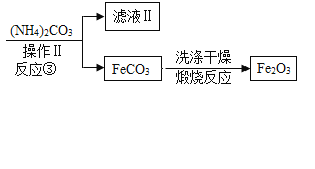
【题目】氯化钙应用广泛,以石灰石(杂质主要是Fe2O3、MgSO4)为原料生产氯化钙的流程如下。
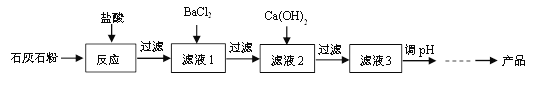
已知:BaCl2 + MgSO4 = BaSO4↓+ MgCl2
Ca(OH)2 + MgCl2 = Mg(OH)2↓+ CaCl2
Ca(OH)2 + FeCl3 = Fe(OH)3↓+ CaCl2
(1)氧化铁与盐酸反应的化学方程式为______。
(2)滤液1中的溶质有HCl、FeCl3、MgSO4和______。
(3)滤液2中加入Ca(OH)2是为了除去______(填序号,下同)。
A.MgCl2 B.FeCl3 C.HCl
(4)滤液3呈碱性,为使溶液pH降低,可加入适量的______。
A.NaCl B.NaOH C.盐酸
【答案】 Fe2O3 + 6HCl = 2FeCl3 + 3H2O CaCl2 ABC C
【解析】(1)氧化铁与盐酸反应生成氯化铁和水,反应的化学方程式为:Fe2O3 + 6HCl = 2FeCl3 + 3H2O;(2)碳酸钙和盐酸反应生成氯化钙、二氧化碳和水;(3)前两步中有盐酸,生成氯化镁、氯化铁,Ca(OH)2能将以上三种杂质除去;(4)盐酸显酸性,能降低溶液pH。

练习册系列答案
相关题目