题目内容
同学们对实验“煅烧石灰石”展开深入探究。
(1)煅烧石灰石。可观察到石灰石的表面 。
(2)为证明石灰石已分解,三位同学从其他角度设计方案如下:
Ⅰ.甲同学按图一所示进行实验(煤气灯亦能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式__ __。
II.乙同学按图二所示进行试验,观察到B中液体变 色,A中实验的作用 。
III.丙同学取一块石灰石进行煅烧,一段时间后发现固体质量减轻mg(即CO2的质量),证明石灰石已分解。
IV.大家认为甲同学的方案不合理,请分析原因 _ 。
(3)为测定石灰石的纯度,丙同学将他刚才煅烧后的固体放入足量稀盐酸中,又产生mg气体,结合上述数据计算可知,丙所取的这块石灰石中含碳酸钙 _ mol(用m表示)。
(1)有气泡产生;(2)Ca(OH)2 +co2 ==CaCO3 ↓+ H2O; 红; 对照试验; 煤气灯中的一氧化碳燃烧会产生二氧化碳,因此使石灰水变浑浊的二氧化碳不一定是碳酸钙分解产生的;(3)m/22
解析试题分析:(1)煅烧石灰石。可观察到石灰石的表面有气泡产生,(2)为证明石灰石已分解Ⅰ.甲同学按图一所示进行实验(煤气灯亦能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式:Ca(OH)2 +co2 ==CaCO3 ↓+ H2O.. II.乙同学按图二所示进行试验,观察到B中液体变红色,A中实验的作用是对照试验,IV.大家认为甲同学的方案不合理,请分析原因煤气灯中的一氧化碳燃烧会产生二氧化碳,因此使石灰水变浑浊的二氧化碳不一定是碳酸钙分解产生的;为测定石灰石的纯度,丙同学将他刚才煅烧后的固体放入足量稀盐酸中,又产生mg气体,结合上述数据计算可知,丙所取的这块石灰石中含碳酸钙mol(用m表示)。(3)因为反应生成的二氧化碳全部来自于碳酸钙,由题意可知生成的二氧化碳的质量为2m克时,可以通过计算碳酸钙中二氧化碳的质量分数计算碳酸钙的质量,进而求出物质的量
考点:氧化钙、氢氧化钙和碳酸钙的转化

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
| 实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| | 20% | 锌粒 | 31.7 |
| | 20% | 锌片 | 50.9 |
| | 30% | 锌粒 | 61.7 |
| | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式 。
(2)小兵用下图装置收集并测量氢气的体积,其中量筒的作用是 。

【收集证据】(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是 。
【得出结论】(4)结论是 。
【评价与反思】
(5)下表是小兵第①组实验的详细数据。
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
请描述锌与硫酸反应的快慢的变化并解释原因 。
(6)锌与硫酸反应的快慢可能还受哪些因素影响? 。
酸、碱、盐是几类有广泛用途的重要化合物.
(1)酸和碱在组成和性质方面有很多共同的特点,请任写出其中的一条.
(2)氢氧化钙是一种常见的碱,列举其在生产、生活中的一种用途.
(3)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如右图)的溶液,他们对此产生了兴趣.
提出问题:这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
①小明根据标签上的组成元素认为一定不可能是 (提示:只有其中一种).
②小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是:
设计实验:为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
| 实验操作 | 实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液 | 出现白色沉淀 |
| 静置一段时间后,倾去上层清液,向沉淀中滴加稀盐酸 | 白色沉淀全部溶解,并产生大量气泡 |
实验反思:④小强认为上述设计实验还可简化,也能达到目的.小强的实验操作是:
(4)若73 g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数.

某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动。
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,溶于水并能与水反应,“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”
【猜想与探究】
猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物
【实验与结论】
| | 实验操作 | 实验现象 | 实验结论 |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水,充分振荡 | | 猜想a、c不成立,猜想b成立。 |
【提出问题】过氧化钠是否为一种制氧剂?与人呼出的哪种气体发生反应?
【提出猜想】过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气。
【进行实验】
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气。

王轩同学设计如下图所示装置:
(1)实验现象及结论:观察到____________现象,判断过氧化钠与氮气没有发生反应。
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气。
华宇同学设计了如下图所示装置
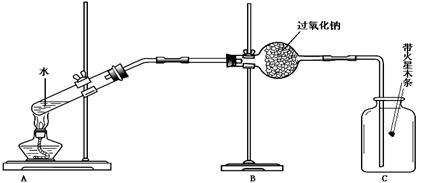
(2)其中A装置的作用是____________。
(3)实验现象及结论:带火星的木条复燃。
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气。李杰在老师的指导下也设计了如下图所示装置。(不考虑稀盐酸的挥发)
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性。 向装置中加入药品。 | | 装置的气密性良好。 |
| ② | 打开分液漏斗活塞,向A装置中缓慢加入稀盐酸。 | A装置中观察到的现象有__________, C装置中有气泡出现。 | A装置中发生反应的化学方程式为________; (2分) |
| ③ | 一段时间后用带火星的木条在D内进行检验。 | 带火星的木条复燃。 | 过氧化钠与二氧化碳反应并生成氧气。 |

(4)实验记录
【实验反思】
张红同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是_____ ___。请你回答如何改进该实验 。
室验室开放日,小明、小佳、小华、小丽等同学来到实验室,看到实验桌上摆放着四瓶无标签的试剂,分别是两瓶固体和两瓶液体,同学们决定对“固体与液体”之间的反应进行一系列探究.
(1)小明同学从一瓶固体和一瓶液体中各取少量试剂于试管中进行混合,立即产生了一种无色气体,对气体是何物质,同学们进行了大胆的猜想,小佳同学的
猜想可能是① ;② ;….
(2)我想设计一个实验证明小佳同学猜想①是正确的,实验设计如下:
| 实验步骤 | 现象及结论 |
| | |
(3)小华想用如图给定的收集装置收集一瓶小佳同学猜想②中的气体,则气体由 (填a或b)端进入.

(4)小丽同学从另外两瓶试剂中各取少量试剂于试管中,发现混合后,固体发生了变化,但无气泡放出.同学们对加入试管中的固体和液体从不同的反应类型、物质类别等方面进行了大胆的猜想:
猜想一: ;
猜想二: ;
猜想三: ;
实验室里某小组正在探究一个问题.根据设计方案,小英向试管中加入2mL氢氧化钠溶液,滴入几滴酚酞溶液,溶液显红色.然后她又用滴管连续滴入一定量的稀硫酸,溶液由红色变为无色.
(1)他们探究的问题是 (填Ⅰ或Ⅱ)
Ⅰ.酚酞溶液遇酸、碱溶液能显示不同颜色吗?Ⅱ.酸和碱溶液能发生反应吗?
(2)大家对小英得到的无色溶液继续探究.
小斌认为反应后溶液中的溶质是硫酸钠,小亮认为溶质有两种,它们是 .
同学们根据以下两种方案进行实验后,一致认为小亮的观点是正确的.请你补填下表的空缺.
| 实验操作 | 实验现象 | 实验结论 |
| 方案一:取少许反应后的溶液置于试管中,向其中加入 | | 小亮的观点正确 |
| 方案二:取少许反应后的溶液置于试管中,向其中加入 | |
(3)请你和全组同学一起分析以下问题.

①稀硫酸和氢氧化钠溶液发生反应的微观过程如图1所示.从粒子的角度具体分析该反应能发生的原因是 .
②锌和硫酸铜溶液发生反应的微观过程如图2所示.从粒子的角度具体分析该变化是化学变化的原因是 .
③通过以上分析,揭示出化学反应的微观本质是 .




