题目内容
【题目】有A、B、C、D四种物质,A是无色、无味的气体;B在A中燃烧发出明亮的蓝紫色火焰,同时生成一种无色、有刺激性气味的气体C;D是一种无色气体,把D通入澄清石灰水中,石灰水变浑浊。试推断A为 ,B为 ,C为 ,D为 。
【答案】(1)氧气 (2)硫 (3)二氧化硫 (4)二氧化碳
【解析】
试题分析:把D通入澄清石灰水中,石灰水变浑浊。说明D是二氧化碳,B在A中燃烧发出明亮的蓝紫色火焰,同时生成一种无色、有刺激性气味的气体C,A是无色、无味的气体,说明C是二氧化硫,B是硫,A是氧气;

【题目】某课外活动小组按右图所示装置制取二氧化碳,并检验二氧化碳的性质:若用装置B来证明二氧化碳与水反应生成碳酸,B中除有少量水外,还应加入的试剂是,当①、②导管口连接时,B中看到的实验现象是:________,其反应的化学方程式为:________。
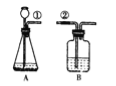
当导管断开一段时间后,看到B中的现象是________,其反应的化学方程式为________.
为测定当地石灰石含碳酸钙的质量分数,该课外活动小组取来一些矿石,并取稀盐酸200g,将其平均分成4份,进行实验,其结果如下:
实验 | 第1份 | 第2份 | 第3份 | 第4份 |
加入样品的质量/g | 5 | 10 | 15 | 20 |
生成CO2的质量/g | 1.54 | 3.08 | 4.4 | m |
依据表中数据请分析计算:
(1)哪几项反应中盐酸有剩余。
(2)上表中m的数值是。
(3)试计算这种石灰石中碳酸钙的质量分数。
【题目】化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】实验所用金属均已用砂纸打磨.
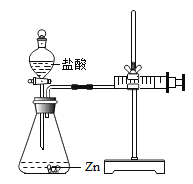
实验(1)为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入等质量、等浓度的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡。写出锌与盐酸发生反应的化学方程式为_______________________.
从实验现象可判断:金属活动性Zn_______Fe(填“<”、’“=”或“>”).
【得出结论】金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是_______.
实验(2)为探究猜想b,小组同学设计如上图的装置进行实验,其中注射器的作用是_______.
所用药品、实验数据如下表:
实验编号 | 选用金属(均取2g) | 盐酸质量分数(均取50mL) | 每分钟产生氢气的体积/mL | |||||
1分钟 | 1﹣2分钟 | 2﹣3分钟 | 3﹣4分钟 | 4﹣5分钟 | 前5分钟共收集气体 | |||
Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【得出结论】金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是_________________.
【反思评价】根据表中实验Ⅱ数据分析,请解释锌与盐酸发生反应由慢到快、再由快到慢的原因是_________________________.
【拓展延伸】通过以上探究,你认为金属与盐酸反应的剧烈程度还可能与哪些因素有关?请你帮助他们继续探究.(只要求提出一种影响快慢的相关假设因素及实验方案)
【假设】________________________________.
【实验方案】_____________________________.