题目内容
兴趣小组将15g含NaCl 90%的粗盐(杂质:泥沙、KNO3)提纯并配制NaCl溶液.试回答: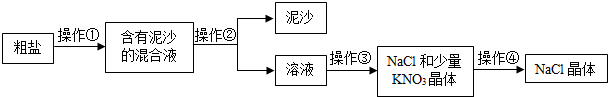
(1)操作②中玻璃棒的作用是 .
(2)操作④中除去KNO3杂质最好选用 .
A.热水 B.冷水 C.NaCl饱和溶液 D.KNO3饱和溶液
(3)提纯获得的NaCl仅12g,由实验操作不当导致产量偏低的原因可能是 (只写一种).
(4)用提纯所得的氯化钠配制100g6%的氯化钠溶液,若实际所配溶液溶质质量分数大于6%,可能是 (填字母编号).
a、天平砝码生锈并沾有污渍 b、用量筒取水时俯视读数
c、用量筒取水时仰视读数 d、配溶液的烧杯刚用蒸馏水润洗过
(5)若用6%的氯化钠溶液,配制50g质量分数为3%的氯化钠溶液,需加水 ml.

(1)操作②中玻璃棒的作用是
(2)操作④中除去KNO3杂质最好选用
A.热水 B.冷水 C.NaCl饱和溶液 D.KNO3饱和溶液
(3)提纯获得的NaCl仅12g,由实验操作不当导致产量偏低的原因可能是
(4)用提纯所得的氯化钠配制100g6%的氯化钠溶液,若实际所配溶液溶质质量分数大于6%,可能是
a、天平砝码生锈并沾有污渍 b、用量筒取水时俯视读数
c、用量筒取水时仰视读数 d、配溶液的烧杯刚用蒸馏水润洗过
(5)若用6%的氯化钠溶液,配制50g质量分数为3%的氯化钠溶液,需加水
考点:氯化钠与粗盐提纯,一定溶质质量分数的溶液的配制,用水稀释改变浓度的方法
专题:溶液、浊液与溶解度,常见的酸 酸的通性
分析:(1)根据玻璃棒具有引流的作用解答;
(2)饱和氯化钠溶液中不能溶解氯化钠,但是能够溶解硝酸钾;
(3)根据溶解时将15g粗盐一次全部倒入水中,立即过滤有没溶解的考虑,固体溅出的后果,提纯后所得精盐尚未完全干燥的后果考虑;
(4)天平砝码沾有杂质时,称量的物质质量会大于需要的质量;用量筒取水时俯视读数,量取的体积会偏小;
(5)稀释前后,溶液中溶质的质量不变.
(2)饱和氯化钠溶液中不能溶解氯化钠,但是能够溶解硝酸钾;
(3)根据溶解时将15g粗盐一次全部倒入水中,立即过滤有没溶解的考虑,固体溅出的后果,提纯后所得精盐尚未完全干燥的后果考虑;
(4)天平砝码沾有杂质时,称量的物质质量会大于需要的质量;用量筒取水时俯视读数,量取的体积会偏小;
(5)稀释前后,溶液中溶质的质量不变.
解答:解:
(1)操作②是固液分离,过滤时玻璃棒具有引流的作用;
(2)热水、硝酸钾饱和溶液都能够溶解氯化钠,而氯化钠饱和溶液不能溶解氯化钠,为了洗去硝酸钾杂质且不造成氯化钠的减少,应该用氯化钠饱和溶液洗涤;
(3)溶解时将15g粗盐一次全部倒入水中,立即过滤,有没溶解的氯化钠被过滤掉了,所以所得精盐少了;蒸发时有一些液体、固体溅出,会导致氯化钠减少,所得精盐比其他同学明显要少;
(4)称量氯化钠所用天平砝码沾有杂质时,称量的氯化钠的质量大于需要的氯化钠的质量,用量筒取水俯视读数时,量取的体积会比需要的体积偏小,这两种情况都会使计算的结果偏大,即都会使实际所配溶液溶质质量分数大于6%.
(5)设需要6%的氯化钠溶液的质量为x,
根据稀释前后,溶液中溶质的质量不变有:x×6%=50g×3%,
x=25g
需加水的质量为:50g-25g=25g,需加水的体积是:
=25cm3=25mL
答案:
(1)引流
(2)C
(3)蒸发时液滴溅出
(4)ab
(5)25
(1)操作②是固液分离,过滤时玻璃棒具有引流的作用;
(2)热水、硝酸钾饱和溶液都能够溶解氯化钠,而氯化钠饱和溶液不能溶解氯化钠,为了洗去硝酸钾杂质且不造成氯化钠的减少,应该用氯化钠饱和溶液洗涤;
(3)溶解时将15g粗盐一次全部倒入水中,立即过滤,有没溶解的氯化钠被过滤掉了,所以所得精盐少了;蒸发时有一些液体、固体溅出,会导致氯化钠减少,所得精盐比其他同学明显要少;
(4)称量氯化钠所用天平砝码沾有杂质时,称量的氯化钠的质量大于需要的氯化钠的质量,用量筒取水俯视读数时,量取的体积会比需要的体积偏小,这两种情况都会使计算的结果偏大,即都会使实际所配溶液溶质质量分数大于6%.
(5)设需要6%的氯化钠溶液的质量为x,
根据稀释前后,溶液中溶质的质量不变有:x×6%=50g×3%,
x=25g
需加水的质量为:50g-25g=25g,需加水的体积是:
| 25g |
| 1g/cm3 |
答案:
(1)引流
(2)C
(3)蒸发时液滴溅出
(4)ab
(5)25
点评:溶本题主要考查粗盐提纯、计算等方面的知识,提纯粗盐时要用到玻璃棒,玻璃棒的用途很广泛,例如可以用来搅拌、引流、转移物质等.

练习册系列答案
相关题目


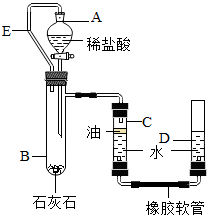 Ⅰ:金属材料用途广泛,回答下列问题:
Ⅰ:金属材料用途广泛,回答下列问题:
 (1)用量筒量取45mL水时,一般采用的量筒规格是
(1)用量筒量取45mL水时,一般采用的量筒规格是