题目内容
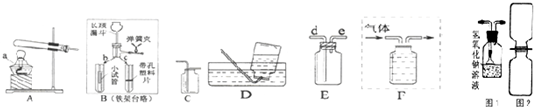
如图是实验室制取和收集气体的装置,请按要求作答:
(1)用B装置制取气体并能随时停止反应,上部与下部对接应选 (填“b”、“c”).
(2)从装置A~D中选择:加热高锰酸钾制取O2并用排水法收集,应选用图中的 (填字母),该反应的符号表达式是: .
(3)若制取O2用F装置排水收集,请将图F补画完整.
(4)实验室要制取NO2气体做微粒运动的演示实验.已知铜片和浓硝酸溶液在常温下反应会生成NO2,同时生成硝酸铜和水.NO2是一种红棕色的气体,密度比空气密度大,易被氢氧化钠溶液吸收,能与水反应生成硝酸和NO.NO2和NO都有毒,易污染环境.
Ⅰ.制取NO2气体的发生装置可选用图中的 (填字母).
Ⅱ.收集NO2可用E装置,NO2气体应从 端(填“d”或“e”)通入.
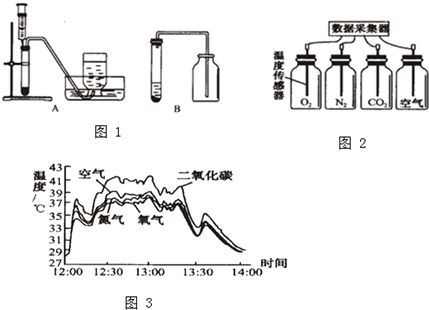
Ⅲ.实验室通常在E装置后还连接一套如图1所示的装置(图中的漏斗可防止液体倒吸),图1装置的主要作用是: .
Ⅳ.利用图2装置,做微粒运动演示实验时,为缩短演示时间,NO2最好盛放在 (填“上”或“下”)面集气瓶中,另一瓶是空气.抽去图2中的玻璃片可看到: .
(1)用B装置制取气体并能随时停止反应,上部与下部对接应选
(2)从装置A~D中选择:加热高锰酸钾制取O2并用排水法收集,应选用图中的
(3)若制取O2用F装置排水收集,请将图F补画完整.
(4)实验室要制取NO2气体做微粒运动的演示实验.已知铜片和浓硝酸溶液在常温下反应会生成NO2,同时生成硝酸铜和水.NO2是一种红棕色的气体,密度比空气密度大,易被氢氧化钠溶液吸收,能与水反应生成硝酸和NO.NO2和NO都有毒,易污染环境.
Ⅰ.制取NO2气体的发生装置可选用图中的
Ⅱ.收集NO2可用E装置,NO2气体应从
Ⅲ.实验室通常在E装置后还连接一套如图1所示的装置(图中的漏斗可防止液体倒吸),图1装置的主要作用是:
Ⅳ.利用图2装置,做微粒运动演示实验时,为缩短演示时间,NO2最好盛放在

考点:氧气的制取装置,氧气的收集方法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)根据用B装置制取气体并能随时停止反应,选择有带孔塑料片的进行分析;
(2)根据高锰酸钾制取氧气的反应物状态和反应条件进行分析;
(3)根据用F装置收集氧气,氧气的密度比水的小,气体应从短管进,以便将水排完收集气体进行分析;
(4)Ⅰ根据制取二氧化氮的反应物状态和反应条件进行分析;
Ⅱ根据二氧化氮密度比空气密度大进行分析;
Ⅲ根据二氧化氮是有毒气体,易被氢氧化钠溶液吸收进行分析;
Ⅳ根据二氧化氮的密度和从分子的性质进行分析.
(2)根据高锰酸钾制取氧气的反应物状态和反应条件进行分析;
(3)根据用F装置收集氧气,氧气的密度比水的小,气体应从短管进,以便将水排完收集气体进行分析;
(4)Ⅰ根据制取二氧化氮的反应物状态和反应条件进行分析;
Ⅱ根据二氧化氮密度比空气密度大进行分析;
Ⅲ根据二氧化氮是有毒气体,易被氢氧化钠溶液吸收进行分析;
Ⅳ根据二氧化氮的密度和从分子的性质进行分析.
解答:解:(1)用B装置制取气体并能随时停止反应,上部与下部对接应选择有带孔塑料片的c试管;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,所以加热高锰酸钾制取O2并用排水法收集,应选用图中的A、D,符号表达式为:2KMnO4
K2MnO4+MnO2+O2↑;
(3)若制取的O2用F装置排水收集,则如图,以便排净瓶内水,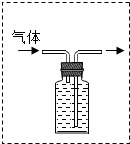 ;
;
(4)Ⅰ、实验室用铜片和浓硝酸溶液在常温下反应会生成NO2,所以制取NO2气体的发生装置可选用图中的B;
Ⅱ、因为NO2密度比空气密度大,用如图1所示的装置收集时,气体应从d端通入;
Ⅲ、因为NO2是有毒气体,易被氢氧化钠溶液吸收,所以图2所示的装置的主要作用是吸收二氧化氮,防止其污染空气;
Ⅳ、一切物质的分子都在不停的运动,将密度大的气体放在上面,密度小的气体放在下面会加快分子运动的速度.
故答案为:(1)c;
(2)A、D,2KMnO4
K2MnO4+MnO2+O2↑;
(3) ;
;
(4)Ⅰ、B;
Ⅱ、d;
Ⅲ、吸收二氧化氮,防止其污染空气;
Ⅳ、上,上瓶气体颜色逐渐变浅,下瓶气体颜色逐渐加深,最后颜色相同.
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,所以加热高锰酸钾制取O2并用排水法收集,应选用图中的A、D,符号表达式为:2KMnO4
| ||
(3)若制取的O2用F装置排水收集,则如图,以便排净瓶内水,
 ;
;(4)Ⅰ、实验室用铜片和浓硝酸溶液在常温下反应会生成NO2,所以制取NO2气体的发生装置可选用图中的B;
Ⅱ、因为NO2密度比空气密度大,用如图1所示的装置收集时,气体应从d端通入;
Ⅲ、因为NO2是有毒气体,易被氢氧化钠溶液吸收,所以图2所示的装置的主要作用是吸收二氧化氮,防止其污染空气;
Ⅳ、一切物质的分子都在不停的运动,将密度大的气体放在上面,密度小的气体放在下面会加快分子运动的速度.
故答案为:(1)c;
(2)A、D,2KMnO4
| ||
(3)
 ;
;(4)Ⅰ、B;
Ⅱ、d;
Ⅲ、吸收二氧化氮,防止其污染空气;
Ⅳ、上,上瓶气体颜色逐渐变浅,下瓶气体颜色逐渐加深,最后颜色相同.
点评:本题主要考查实验室制取和收集氧气,以及二氧化氮的物理、化学性质,需要通过所学知识和题干信息分析解题,需要同学们学好基础知识,以不变应万变.

练习册系列答案
相关题目
下列除杂质的方法不正确的是( )
| 选 项 | 物 质 | 杂 质 | 除杂方法 |
| A | CaO | CaCO3 | 加适量的稀盐酸 |
| B | CaCO3 | KNO3 | 溶解、过滤 |
| C | N2 | O2 | 通过灼热的铜网 |
| D | NaCl | NH4HCO3 | 加热 |
| A、A | B、B | C、C | D、D |
如图为某反应的微观示意图,下列说法正确的是( )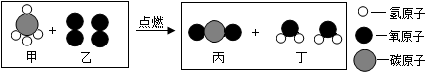

| A、甲物质中碳元素的质量分数为75.0% |
| B、甲和丙都是有机物 |
| C、该反应是置换反应 |
| D、反应前后氧元素的化合价未发生改变 |
 某学习小组为探究空气中氧气的含量,设计了如图所示的装置,根据装置回答下列问题:
某学习小组为探究空气中氧气的含量,设计了如图所示的装置,根据装置回答下列问题: X、Y、Z、甲、乙、丙均为初中化学中常见的物质,其中X、Y、Z为单质,Z为红色固体,甲、乙、丙为氧化物,X、丙为黑色固体.它们之间在一定条件下存在如图所示的转化关系.
X、Y、Z、甲、乙、丙均为初中化学中常见的物质,其中X、Y、Z为单质,Z为红色固体,甲、乙、丙为氧化物,X、丙为黑色固体.它们之间在一定条件下存在如图所示的转化关系.