题目内容
【题目】硅酸钠(Na2SiO3)是我国优先发展的精细化学产品。用某种石英砂矿石(主要成分是SiO2,还含有少量的CuO、Na2SO4、Na2CO3)。工业上制备硅酸钠晶体的流程如下:查阅资料:SiO2既不溶于水,也不与盐酸反应;Na2SO4、Na2CO3均易溶于水。请问答:
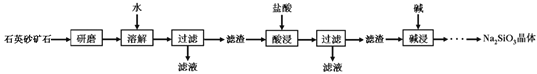
(1)“研磨”的目的是__________________________________;
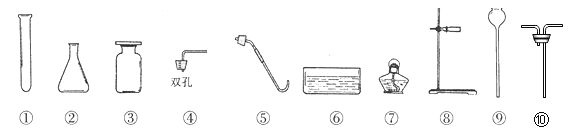
(2)实验室的过滤操作中必须用到的玻璃仪器有:烧杯、漏斗、________,过滤时发现过滤速率缓慢,可能原因是______________________________;
(3)“酸浸”过程中发生反应的化学方程式为_________________________;
(4)“碱浸”时加入的碱液应选用_________________(填化学式)溶液。
【答案】 加速溶解(或加大反应物之间的接触面积或加快反应速率) 玻璃棒 滤纸没有紧贴漏斗内壁 CuO+2HCl![]() CuCl2+H2O NaOH
CuCl2+H2O NaOH
【解析】(1)由于反应物之间接触越充分反应越快,同时颗粒越小,溶解也就越快,所以“研磨”的目的是加速溶解(或加大反应物之间的接触面积或加快反应速率);(2) 实验室的过滤操作中必须用到的玻璃仪器有:烧杯、漏斗、玻璃棒,过滤时发现过滤速率缓慢,可能原因是:滤纸没有紧贴漏斗内壁;(3)“酸浸”是除去氧化铜,是氧化铜和硫酸反应生成硫酸铜和水,对应的化学方程式为CuO+2HCl![]() CuCl2+H2O;(4)“碱浸”是二氧化硅和氢氧化钠反应,生成硅酸钠和水,对应的化学方程式为SiO2+2NaOH=H2O+Na2SiO3,“碱浸”时加入的碱液应选用NaOH。
CuCl2+H2O;(4)“碱浸”是二氧化硅和氢氧化钠反应,生成硅酸钠和水,对应的化学方程式为SiO2+2NaOH=H2O+Na2SiO3,“碱浸”时加入的碱液应选用NaOH。

【题目】密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表所示。下列说法正确的是![]()
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量(克) | 50 | 11 | 15 | 32 |
反应后质量(克) | 64 | M | 5 | 28 |
A. 该反应是化合反应
B. M的值是15
C. 乙一定是催化剂
D. 反应中甲、丁质量比为16 :7