题目内容
【题目】(4分)在氯化钙和氯化钠的混合物中加入一定量的水,全部溶解得到50克混合溶液,向该溶液中逐滴加入一定溶质质量分数的碳酸钠溶液,生成沉淀与加入碳酸钠溶液的质量关系如图所示、计算:
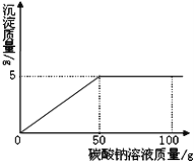
(1)所加碳酸钠溶液的溶质质量分数
(2)若恰好完全反应时所得溶液的溶质质量分数为10%,则原固体混合物的质量是多少?
【答案】(1)10.6%;(2) 8.95g
【解析】
试题分析:(1)由图象可知,CaCO3的质量为5g,
设原混合物中碳酸钠的质量为x,生成氯化钠的质量为y、
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
x 5g y
![]() =
=![]() =
=![]()
x=5.3g,y=5.85g
所加碳酸钠溶液的溶质质量分数为![]() ×100%=10.6%
×100%=10.6%
(2)原固体混合物的质量是w
所以![]() ×100%=10%
×100%=10%
w=8.95g
答:(1)所加碳酸钠溶液的溶质质量分数为10.6%
(2)原固体混合物的质量是8.95g

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案
相关题目