题目内容
【题目】书写化学方程式:
(1)电解水_____。
(2)氢气燃烧_____。
(3)二氧化碳和水反应_____。
(4)二氧化碳和石灰水反应_____。
(5)甲烷充分燃烧_____。
(6)乙炔充分燃烧_____。
(7)硝酸银与盐酸反应_____。
(8)电解氯化镁_____。
(9)铝的燃烧_____。
(10)一氧化碳还原氧化铁_____。
【答案】2H2O![]() 2H2↑+O2↑ 2H2+O2
2H2↑+O2↑ 2H2+O2![]() 2H2O CO2+H2O=H2CO3 CO2+Ca(OH)2=CaCO3↓+H2O CH4+2O2
2H2O CO2+H2O=H2CO3 CO2+Ca(OH)2=CaCO3↓+H2O CH4+2O2![]() CO2+2H2O 2C2H2+5O2
CO2+2H2O 2C2H2+5O2![]() 4CO2+2H2O NaCl+AgNO3=AgCl↓+NaNO3 MgCl2
4CO2+2H2O NaCl+AgNO3=AgCl↓+NaNO3 MgCl2![]() Mg+Cl2↑ 4Al+3O2
Mg+Cl2↑ 4Al+3O2![]() 2Al2O3 3CO+Fe2O3
2Al2O3 3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
【解析】
(1)电解水生成氢气和氧气;故填:2H2O![]() 2H2↑+O2↑。
2H2↑+O2↑。
(2)氢气与氧气在点燃的条件下反应生成水;故填:2H2+O2![]() 2H2O。
2H2O。
(3)二氧化碳和水反应生成碳酸;故填:CO2+H2O=H2CO3。
(4)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水;故填:CO2+Ca(OH)2=CaCO3↓+H2O。
(5)甲烷与氧气在点燃的条件下反应生成二氧化碳和水;故填:CH4+2O2![]() CO2+2H2O。
CO2+2H2O。
(6)乙炔与氧气在点燃的条件下反应生成二氧化碳和水;故填:2C2H2+5O2![]() 4CO2+2H2O。
4CO2+2H2O。
(7)硝酸银与盐酸反应生成氯化银沉淀和硝酸钠;故填:NaCl+AgNO3=AgCl↓+NaNO3。
(8)氯化镁在通电的条件下分解为镁和氯气;故填:MgCl2![]() Mg+Cl2↑。
Mg+Cl2↑。
(9)铝与氧气在点燃的条件下反应生成氧化铝;故填:4Al+3O2![]() 2Al2O3。
2Al2O3。
(10)在高温的条件下,一氧化碳还原氧化铁生成铁,同时生成二氧化碳;故填:3CO+Fe2O3![]() 2Fe+3CO2。
2Fe+3CO2。

 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案【题目】某化学课堂围绕“酸碱中和反应”,将学生分成若干小组开展探究活动。请你和他们一起完成以下实验探究。(包括表中空格)。
(演示实验)将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中。该反应的化学方程式为______。
(提出问题)实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么?
(猜想与假设)针对疑问,大家纷纷提出猜想。甲组同学的猜想如下,请你补上猜想四。
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4、H2SO4和NaOH
猜想四:______。
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的。请指出不合理的猜想并说明理由,______。
(实验探究)
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有______。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用了老师提供的pH试纸、Na2CO3溶液、BaC12溶液,进行如下三个方案的探究。请完成实验报告:
实验方案 | 测溶液的pH | 滴加Na2CO3溶液 | 滴加BaC12溶液 |
实验操作 |
|
|
|
实验现象 | 试纸变色,对比比色卡,pH<7 | ______ | 产生白色沉淀 |
实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
(得出结论)通过探究,全班同学一致确定猜想二是正确的。
(评价反思)(1)老师对同学们能用多种方法进行探究,并且得出正确结论给予了肯定。同时指出[实验探究](2)中存在两处明显错误,请大家反思。同学们经过反思发现了如下两处错误:
①实验操作中的错误是______;
②实验方案中也有一个是错误的,错误的原因是______。
(2)在分析反应后所得溶液中溶质成分时,除了考虑生成物外,还需要考虑______。
【题目】某化工厂用废硫酸制备K2SO4的流程如下:
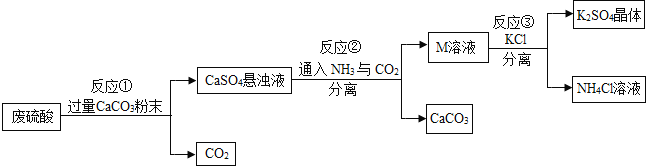
物质 | KCl | K2SO4 | NH4Cl | (NH4)2SO4 |
溶解度/g(20℃) | 34.2 | 11.1 | 37.2 | 75.4 |
(1)生产上将CaCO3研成粉末的目的是______。
(2)上述流程中,除可综合利用CO2外,还可循环使用的物质是______(填化学式)。
(3)写出反应①的化学方程式:______。写出反应②的化学方程式:______。
(4)反应③中相关物质的溶解度如表所示。反应③在常温下能实现的原因是______。
(5)洗涤反应③所得晶体不用水而用饱和K2SO4溶液的目的是______。