题目内容
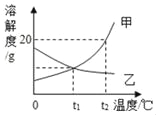
【题目】如图是甲、乙两种固体物质的溶解度曲线,请回答:
(1)在___时,甲、乙两种物质的溶解度相同。
(2)不改变溶剂的质量,将t1℃甲的饱和溶液变为不饱和溶液可 采用方法是___。
(3)t2℃时,将25g甲放入装有100g水中,充分搅拌发现固体先全部溶解,一段时间后又有晶体析出,请解释甲固体全部溶解的原因___。
(4)下列有关说法正确的是___(填序号)。
①甲中含有少量的乙可采用降温结晶的方法提纯甲
②t2℃时,甲溶液的溶质质量分数比乙溶液溶质质量分数大
③t2℃时,将等质量甲、乙分别加水配成饱和溶液,所得甲溶液质量比乙溶液小
④将t2℃时甲、乙饱和溶液降温至t1℃时,所得甲、乙溶液的溶质质量分数相等
⑤将t2℃时120g甲的饱和溶液降温至t1℃时,可析出20g甲晶体
【答案】t1℃ 减少溶质(即降低温度、过滤,再恢复到原温度) 是甲固体溶于水温度升高 ①③
【解析】
(1)在t1℃时,甲、乙两种物质的溶解度相同,因为该温度下,它们有交点;故答案为:t1℃;
(2)不改变溶剂的质量,将t1℃甲的饱和溶液变为不饱和溶液可采用方法是:减少溶质(即降低温度、过滤,再恢复到原温度);故答案为:减少溶质(即降低温度、过滤,再恢复到原温度);
(3)t2℃时,将25g甲放入装有100g水中,充分搅拌发现固体先全部溶解,一段时间后又 有晶体析出,原因是甲固体溶于水温度升高;故答案为:是甲固体溶于水温度升高;
(4)有关说法正确的是:①甲中含有少量的乙可采用降温结晶的方法提纯甲,选项正确;
②t2℃时,甲的溶解度比乙大,只能说明甲的饱和溶液质量分数比乙饱和溶液质量分数大,选项错误;
③t2℃时,将等质量甲、乙分别加水配成饱和溶液,所得甲溶液质量比乙溶液小,正确;
④将t2℃时甲、乙饱和溶液降温至 t1℃时,所得甲、乙溶液的溶质质量分数是甲大于乙,错误;
⑤将t2℃时甲的溶解度是20g,120g甲的饱和溶液中含有20g甲和100g水,降温至t1℃时,由于t1℃时甲的溶解度不为零,则不可能析出20g甲晶体,故答案为:①③。