题目内容
【题目】下图是实验室中常见装置,回答下列问题。
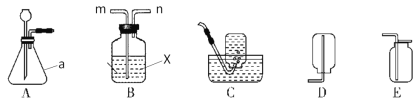
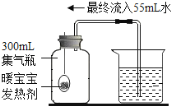
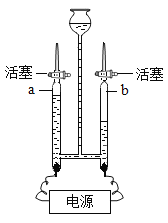
(1)仪器a的名称是__________________
(2)用装置A进行实验时,首先应________________(填序号)
①加药品②加热 ③检查装置气密性
(3)用A装置制取气体的不足之处是____________________________
(4)若要收集干燥的CO2,可将含有水蒸气的CO2从装置B的______(填“m”成“n”)端导入,试剂X是________;再用装置______(填“C”或“D”或“E”)收集。
(5)向集满CO2的集气瓶中加入澄清石灰水,反应的化学方程式为___________________
【答案】锥形瓶 ③ 不能随时控制反应的发生与停止 m 浓硫酸 E CO2+ Ca(OH)2=CaCO3↓+H2O
【解析】
(1)由图可知,仪器a的名称是锥形瓶,故填锥形瓶。
(2)制取气体时,实验前应先检查装置气密性,故填③。
(3)A装置进行实验时不能随时控制反应的发生与停止,故填不能随时控制反应的发生与停止。
(4)收集干燥的CO2,应将含有水蒸气的CO2从装置B的长管,即m端通入到干燥剂中,使水蒸气被充分吸收,故填m;
浓硫酸具有吸水性,所以可用浓硫酸作为干燥剂来干燥气体,故填浓硫酸;
氧气的密度大于空气的密度,所以再用向上排空气法收集干燥后的氧气,故填E。
(5)二氧化碳能与澄清石灰水中的氢氧化钙反应生成水和碳酸钙沉淀,使澄清石灰水变浑浊,故反应的化学方程式写为:CO2+Ca(OH)2= CaCO3↓+H2O。

【题目】在密闭容器有甲、乙、丙、丁四种物质,在一定条件下让其充分反应,测得反应前后各物质的质量变化如下表所示:
物 质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量/g | 50 | 23 | 1 | 3 |
反应后的质量/g | 2 | x | 45 | 30 |
下列说法中,正确的是
A.甲一定是化合物B.x的值等于0
C.丙和丁的质量变化比为3:2D.该反应是分解反应
【题目】化学实验活动课上,同学们利用了如图所示实验探究氢氧化钙的性质。
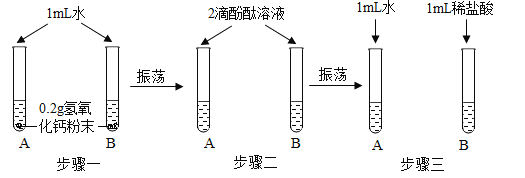
(1)上述三个步骤的A试管中固体始终无明显减少,那么能说明A试管的水中溶有氢氧化钙的现象是__________。
(2)步骤三试管B中溶液变无色,发生反应的化学方程式_______________。
小明的实验:小明直接把稀盐酸滴入盛有氢氧化钙溶液的试管中,始终没有看到明显变化。
(提出问题)小明实验后试管中溶质的成分是什么?
(查阅资料)CaCl2溶液显中性。
(猜想与假设)针对疑问,甲组同学猜想如下:
猜想I:只有CaCl2猜想Ⅱ有________
猜想Ⅲ:有CaCl2和Ca(OH)2
猜想Ⅳ:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是_____________
(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
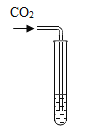
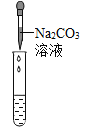
实验方案 | 滴加紫色石蕊试液 | 通入CO2 | 滴加Na2CO3 |
实验操作 |
|
|
|
实验现象 | _________ | __________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出结论)通过探究,全班同学一致确定猜想Ⅲ是正确的。
(评价反思)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因_____________。