题目内容
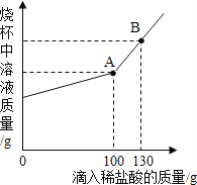
【题目】如图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是( )
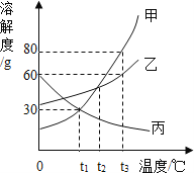
A.t1℃时,30g甲物质溶于70g水中得到30%的甲溶液
B.t3℃时将甲、乙两物质的饱和溶液降温到t2℃,析出晶体质量甲>乙
C.t2℃时,甲、丙溶液中溶质的质量分数甲>乙
D.将t3℃时甲、乙、丙三种物质的饱和溶液降温到t1℃,所得溶液溶质的质量分数关系是乙>甲>丙
【答案】D
【解析】
A、t1℃时,甲物质的溶解度是30g,所以30g甲物质溶于70g水中,物质甲溶解的质量为70g×![]() =21g,所以所得饱和溶液的质量分数为:
=21g,所以所得饱和溶液的质量分数为:![]() ×100%=23.1%,所以不能得到30%的甲溶液,故A错误;
×100%=23.1%,所以不能得到30%的甲溶液,故A错误;
B、t3℃时,将甲、乙两物质的饱和溶液降温到t2℃,饱和溶液的质量不能确定,所以析出晶体质量也不能确定,故B错误;
C、t2℃时,甲、丙溶液的状态不能确定,所以溶液中溶质的质量分数也不能确定,故C错误;
D、t1℃时,乙物质的溶解度最大,甲物质的溶解度次之,降低温度,甲、乙物质会析出晶体,丙物质不会析出晶体,应该按照t3℃时的溶解度进行计算,所以将t3℃时甲、乙、丙三种物质的饱和溶液降温到t1℃,所得溶液溶质的质量分数关系是乙>甲>丙,故D正确。
故选:D。

【题目】有一种管道疏通剂,主要成分为铝粉和氢氧化钠混合粉末。工作原理是:利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对毛发等淤积物的腐蚀,同时产生氢气增加管道内的气压,利于疏通。小柯利用如图装置测定疏通剂中铝的质量分数。
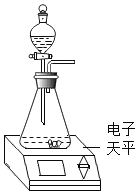
Ⅰ.取样品20g,倒入容积为200ml的锥形瓶中,然后在分液漏斗中加入水,置于电子天平上测出总质量m1。
Ⅱ.打开活塞,加入足量的水充分反应,直到没有固体剩余,静置一段时间,测出总质量m2。
Ⅲ.实验数据如下表:
反应前总质量m1 | 反应后总质量m2 |
371.84g | 371.24g |
回答下列问题:
(1)配平化学方程式:2Al+2NaOH+2H2O![]() ______NaAlO2+3H2↑
______NaAlO2+3H2↑
(2)根据化学方程式计算样品中铝的质量分数。______
(3)以下情形会导致样品中铝的质量分数测量结果偏高的原因可能有______。
A向锥形瓶中倒入样品时,撒出了部分粉末
B在反应过程中有水蒸气逸出
C没有等装置中氢气全部排尽就称量