题目内容
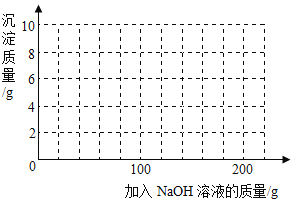
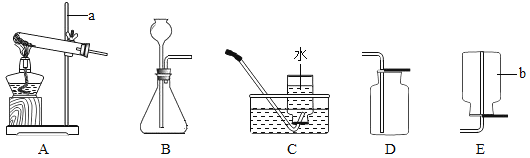
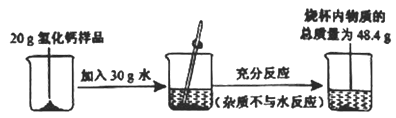
【题目】某化学兴趣小组在实验室用碳酸钠溶液和熟石灰制取少量氢氧化钠溶液,他们的实验过程和相关数据如图所示。请计算:
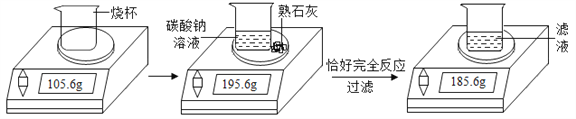
(1)实验中生成沉淀的质量为________g;
(2)所得氢氧化钠溶液中溶质的质量分数。
(反应的化学方程式:Na2CO3+Ca(OH)2==CaCO3↓+2NaOH)
【答案】(1)10;(2)10%
【解析】
(1)实验中生成沉淀的质量为:195.6g-185.6g=10g
(2)设所得氢氧化钠溶液中溶质的质量为x
Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH
100 80
10g x
![]() =
=![]() 解得x=8g
解得x=8g![]()
反应后所得溶液的质量是:185.6g-105.6g=80g
故所得氢氧化钠溶液中溶质的质量分数为:![]() ×100%=10%
×100%=10%

【题目】酸和碱在生产生活及科学研究中有着重要的作用。
(1)某危险品运输车辆发生交通事故,造成浓硫酸泄漏,消防官兵向事故现场撒入大量的白色粉末来做中和处理,以免发生由此造成的环境污染。请写出有关反应的化学方程式:______________________。
(2)化学兴趣小组的同学向盛有稀氢氧化钠溶液的烧杯中倒入一定量的稀盐酸时,没有观察到明显现象。同学们就此做了如下探究:
①小组同学对烧杯内溶液中的溶质成分进行了如下猜想,其中不合理的是______________________。
A 氢氧化钠、氯化氢 B 氯化钠 C 氯化钠、氯化氢 D 氯化钠、氢氧化钠
②为了证明氢氧化钠溶液和稀盐酸混合后确实发生了化学反应,甲同学设计如下实验,并把反应后的溶液蒸干,得到一些白色固体。
实验操作 | 实验现象 | 白色固体成分 |
取少量氢氧化钠溶液于试管中,离加2-3滴无色酚酞溶液,然后逐滴滴加稀盐酸,滴加几滴后用pH计测定溶液的酸碱度 | 溶液先显红色,pH >7 | _____ |
溶液后显无色,pH_______7 | NaCl |
结论:没有明显现象发生的化学反应,可以借助酸碱指示剂或pH计来确定反应的发生。
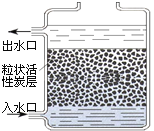
③乙同学为了确定反应后所得溶液中溶质的成分,取少量溶液滴入几滴酚酞溶液,观察到溶液仍为无色。则烧杯内溶液中的溶质可能是①中的_______,为了继续探究烧杯内溶质的成分,乙同学认为可以选用铁、碳酸钠、氧化铜等多种试剂。请你分析该同学选用这些试剂的依据是什么?____________________
④区分无色溶液氢氧化钠和澄清石灰水的过程中,写出有明显现象发生的化学方程式。____________________
(3)如图某钙片可缓解胃酸过多症。若按用量服用,理论上每天可以消耗氯化氢的质量是多少? (保留一位小数)__________

【题目】现有H2SO4与CuSO4的混合溶液,为了分析混合溶液中H2SO4与CuSO4的质量分数,设计如下实验方案:取四份混合溶液各100 g,分别缓慢加入到50 g、100 g、150 g、200 g某NaOH溶液中,测得四组实验数据如下表:
第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | 第Ⅳ组 | |
NaOH溶液的质量/g | 50 | 100 | 150 | 200 |
生成沉淀的质量/g | 0 | 2.45 | 7.35 | 9.8 |
(1)100 g混合溶液与NaOH溶液完全反应生成沉淀的质量为_______g。
(2)混合溶液中CuSO4的溶质质量分数是多少?(写出计算过程)
(3)混合溶液中H2SO4的溶质质量分数为___________。
(4)若在100 g混合溶液中不断加入上述NaOH的溶液,请画出加入NaOH溶液的质量与所产生沉淀质量的关系图。(在答题卡的坐标图中作图)