题目内容
【题目】阅读下面科普短文
碳元素是最早被人类认识和利用的元素。碳元素在地球上虽然广泛分布,但其含量不足0.03%。碳元素是一切有机体骨架的组成元素,在人体中的含量约占 18%。主要以有机含碳化合物形式存在,如糖类、蛋白质等。人体中的无机含碳化合物种类较少,在血浆中主要以碳酸氢盐缓冲系统 (H2CO3/HCO3-)的形式存在。迄今为止,发现了 15 种碳原子,它们在元素周期表中占据如图 1 所示的同一个“格”,其中 C-12 和C-13 属于稳定型,考古研究中,通过测定 C-14 含量估算古物的年代。20 世纪起,人类对碳元素的认识突飞猛进。下表列出了与之相关的主要事件:碳的这些新型结构的发现和性能研究的发展,使其广泛应用于工业、材料、生物医学等领域。依据文章内容回答下列问题:

时间 | 40 年代 | 1967 年 | 1969 年 | 1985 年 | 1991 年 | 21 世纪 |
事件 | 发现C-14 | 发现六角金刚 石和单斜超硬 碳 | 发现银白色的白炭 | 发现富勒烯 的第一个成 员 C60(图 2) | 发现碳纳米管(图 3) | 从石墨中剥离出仅 由一层碳原子构成 的薄片-石墨烯(图4) |
(1)碳在人体中的存在形式有_______ 种;
(2)关于图 1 所示的相关信息分析,错误的是________;
A 原子序数为 6 B 电子数为 12 C 元素符号为 C
(3)结合你所学的知识,你认为原子 C-12 和 C-13 的不同点是________;
A 质子数不同 B 电子数不同 C 中子数不同
(4)从石墨中剥离出来的石墨烯具有优良的各种性能,被认为是一种未来革命性的材料。石墨和金刚石的物理性质不同的原因是________;
(5)富勒烯 C60 中数字“60”的含义是________。
【答案】2 B C 碳原子的排列方式不同 一个 C60 分子中有 60 个碳原子
【解析】
(1)由题干信息可知,碳在人体内主要以有机含碳化合物形式和碳酸氢盐缓冲系统(H2CO3/HCO3-)的形式存在;
(2)A、元素周期表中的一格可知:左上角的数字表示原子序数。碳的原子序数为6,故A正确;
B、原子序数=质子数=核外电子数,所以碳原子的电子数为6,故B错误;
C、元素周期表中的一格可知:字母表示该元素的元素符号。碳的元素符号为C,故C正确。故选B;
(3)C-12和C-13的质子数相同,中子数不同;故选C;
(4)石墨中碳原子排列成平面层状结构,金刚石中碳原子排列成立体网状结构,二者物理性质不同的原因是碳原子的排列方式不同;
(5)根据化学式的意义可知,C60的含义是一个C60 分子中有 60个碳原子。

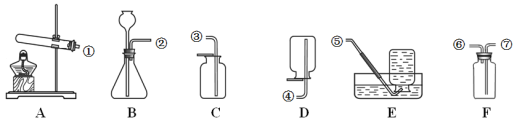
【题目】根据下列仪器装置,回答有关问题。
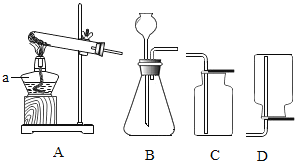
(1)制取氧气。实验室选用装置A制取氧气时,用到的化学药品是__________ (用化学式表示);实验结束熄灭酒精灯的操作为__________。
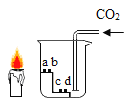
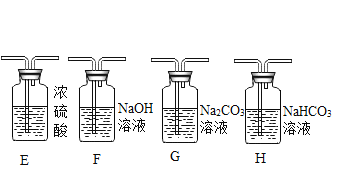
(2)制取二氧化碳。用一定浓度的盐酸与石灰石反应制取二氧化碳气体,发生反应的化学方程式为_______________。为制得干燥、纯净的二氧化碳气体,所选装置的连接顺序为_____→ H → _____ →干燥、纯净CO2 (在横线内填装置序号)。
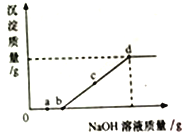
(3)进一步探究二氧化碳与氢氧化钠溶液的反应。
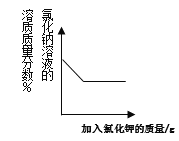
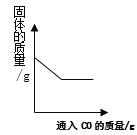
(提出问题)制取干燥、纯净的二氧化碳气体流程中,选用装置H而不用G,因为碳酸钠溶液中通入二氧化碳发生反应:Na2CO3 + CO2 + H2O = 2NaHCO3。向氢氧化钠溶液中通入一定量二氧化碳后,所得溶液中溶质是什么?
(查阅资料)碳酸氢钠与氢氧化钠发生反应:NaOH+NaHCO3 =Na2CO3 + H2O;Ca(HCO3)2溶于水。
(猜想)所得溶液中的溶质是:I.Na2CO3;II.NaHCO3;III.Na2CO3和NaHCO3;IV._____。
(实验)请你参与下列验证猜想③的实验,完成探究报告。
步骤和方法 | 现象 | 分析 |
取少量反应后的溶液,加入足量的CaCl2溶液 | __________ | 发生反应的方程式:_____ |
__________ | 产生白色沉淀 | 结论:猜想III正确 |
(讨论)二氧化碳通入一定量的氢氧化钠溶液,影响反应后生成物成分的决定因素是________。