题目内容
【题目】下列图象反映的变化规律与其对应操作不相符的是
A. 向氯化钠的饱和溶液中加入氯化钾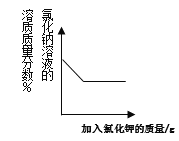
B. 向灼热的赤铁矿中通入CO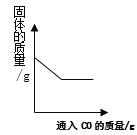
C. 向等质量的Al和Mg中加入足量的等质量等溶质质量分数的稀盐酸
D. 将饱和的氯化钠溶液恒温蒸发水
【答案】D
【解析】
A、向氯化钠的饱和溶液中加入氯化钾,氯化钾溶解,溶液的质量增加,所以溶液中氯化钠的质量分数逐渐减小直至氯化钾也形成饱和溶液,选项正确;
B、向灼热的赤铁矿中通入CO,CO夺取氧化铁中的氧元素形成二氧化碳气体挥发,固体的质量不断减少,直至氧化铁完全反应,选项正确;
C、参加反应的等质量的稀盐酸与金属单质反应生成等质量的氢气,等质量的Al和Mg与足量的稀盐酸反应后Al与酸反应生成的氢气的质量大,选项正确;
D、将饱和的氯化钠溶液恒温蒸发水,温度不变,溶解度不变,剩余溶液仍为该温度下的饱和的氯化钠溶液,则溶液中氯化钠的质量分数保持不变,选项错误,故选D。

 综合自测系列答案
综合自测系列答案【题目】红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”。其标签如图所示,某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究。
品名:504双吸剂
成分:铁粉、生石灰等
(提出问题):久置固体的成分是什么?
(查阅资料):铁与氯化铁溶液在常温下发生反应:Fe+2FeCl3=3FeCl2打开固体包装观察:部分固体呈黑色,部分固体呈白色,另有少量红棕色的块状固体。
(作出猜想):久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。其中可能含有Fe2O3的依据是_____________。
(实验探究):甲同学的方案:
实验操作 | 实验现象 | 实验结论 |
(1)取少量久置固体于试管中,滴加足量的蒸馏水,搅拌 | 固体溶解,试管外壁发烫 | 固体中一定含有______ |
(2)过滤,在滤液中滴加无色酚酞溶液 | 溶液变红色 | 固体中一定含有氢氧化钙 |
(3)取滤渣放入试管中,滴加足量的________ | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有______,一定不含氧化铁 |
(实验质疑)乙同学认为甲同学在实验中得出“一定不含氧化铁”的结论是错误的,理由是______________。你认为甲同学哪一步实验操作得出的结论也不合理:__________,理由是___________(用化学方程式表示。)
(继续探究)乙同学另取久置的固体进行实验探究:
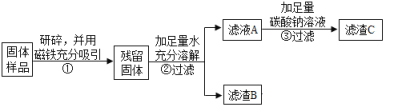
乙同学对滤渣B进行探究:
实验操作 | 实验现象 | 实验结论 |
取滤渣B于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、______有气泡冒出、______ | 固体中一定含有CaCO3和Fe2O3。写出Fe2O3和稀盐酸反应的化学方程式_______ |
(计算得出结论):如上述实验流程,乙同学现取5g久置固体研碎,用磁铁吸引,得残留固体3g,加足量水充分溶解过滤,得滤渣B的质量为1.8g。在滤液A中加足量碳酸钠溶液后过滤得滤渣C的质量为2g,通过计算后得出残留固体的成分为:__________。
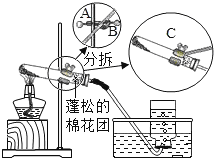
【题目】2019年苏州市初中化学实验考查内容是“用高锰酸钾制取氧气”(装置图如下),下面是某同学在本次实验过程中填写的部分实验报告,请回答有关问题:
实验步骤 | 有关问题 |
⑴检查气体发生装置的气密性。 | 检查装置气密性的具体操作及气密性良好的判断依据是_____。 |
⑵向试管中加入少量高锰酸钾粉末,使其平铺于试管底部,按上图所示组装实验装置。在接近试管口的地方放置一小团蓬松的棉花团。 | ①用药匙或纸槽向试管中加入少量高锰酸钾粉末。 ②组装实验装置时,要根据___的高度将盛有药品的试管固定在铁架台上。 ③欲调整装置中试管的倾斜角度,应调节图中A、B、C哪个旋钮:___旋钮。 ④试管口棉花团的作用是____。 |
实验步骤 | 有关问题 |
⑶加热试管,当导管口有连续均匀气泡冒出时,开始收集气体。 | ①加热试管的方法是____。 ②发生反应的化学方程式为____。 ③收集满瓶氧气的操作过程是:等集气瓶中的水排完后,一只手扶稳集气瓶,另一只手首先小心地将导管从瓶口移开,然后___,最后把集气瓶正放在桌子上。 |
⑷气体收集完毕后,操作B | 操作B是先____,再_____ |
⑸收集完气体后,测得其纯度明显偏低,其原因可能是____(填字母)。
A 高锰酸钾中混入了二氧化锰 B 收集前,集气瓶中未注满水
C 收集后,集气瓶中仍留有水 D 未见气泡连续均匀冒出时就开始收集
⑹选择排水法收集一瓶氧气,供“铁丝在氧气中燃烧”实验使用的理由是____。
⑺)加热3.16g高锰酸钾固体一段时间,若高锰酸钾中的氧元素有1/4转化为氧气,则生成的氧气的质量为____,剩余固体中氧元素的质量分数为____。(精确到0.1%)
⑻林同学称取一定质量高锰酸钾制取一定质量的氧气,将温度控制在250℃加热制O2,实验结束时,林同学发现在用高锰酸钾制取氧气的实验中,收集到的O2大于理论产量,针对这一现象,同学们在老师的指导下进行了如下探究:
(提出猜想)依据质量守恒定律,他们做出如下猜想:
猜想Ⅰ:反应生成的MnO2分解放出O2
猜想Ⅱ:反应生成的K2MnO4分解放出O2
(实验验证)同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变。则猜想____错误。
②第二组同学取一定质量的K2MnO4在250℃条件下加热,固体质量____(填“减轻”或“增重”),得出了猜想Ⅱ正确的结论。
林同学提出:不用测定质量也能验证以上猜想是否正确,林同学选择的实验方法可能是____。
(拓展延伸)实验发现,K2MnO4受热只能部分分解,经分析可能是K2MnO4分解的生成物K2O对其分解产生影响。为验证此结论,设计如下实验方案:
①分别取K2MnO4固体于两支试管中,一支试管中加入K2O,一支试管中不加K2O。
②加热,用相同规格的集气瓶,用排水法分别收集一瓶气体。③比较所用的时间长短,以确定锰酸钾的分解是否与氧化钾有关系。该过程中还必须控制相同的变量是______。