题目内容
【题目】某化学兴趣小组的同学在做酸碱中和反应时,将稀盐酸滴加到盛有氢氧化钠溶液的试管中,没有观察到明显现象(氢氧化钠未变质),小组同学对氢氧化钠溶液与稀盐酸是否发生了化学反应产生了兴趣,他们做了如下实验
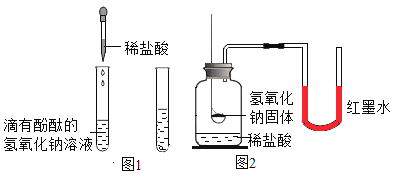
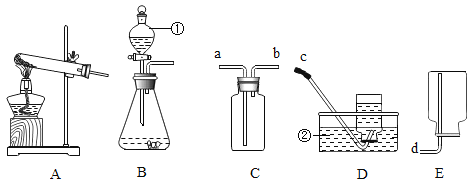
(实验一)酚酞溶液在酸和碱溶液中显示不同的颜色,可借助指示剂的颜色变化判断酸碱是否发生了反应,如图 1所示
(1)可说明试管中两种物质发生反应的现象是_____,该反应的化学方程式为_____
(实验二)化学反应通常伴随能量的变化,可借助反应前后的温度变化来判断酸碱是否发生了反应,如图2所示
(2)将盛有氢氧化钠固体的燃烧匙伸入稀盐酸中,观察到U形管中右侧红墨水液面上升,该现象_____(填“能”或“不能”)证明氢氧化钠与稀盐酸发生了化学反应,理由是_____
(3)小组同学利用温度传感器测定了盐酸与氢氧化钠反应的时间 -温度曲线如图3所示
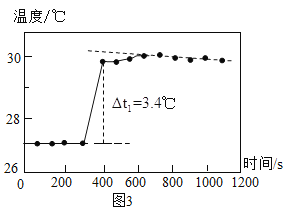
①由曲线变化情况分析可知,稀盐酸与氢氧化钠溶液发生反应并_____(填 “放出”或“吸收”)热量
② 400秒后,曲线开始呈下降趋势的原因是_____
(实验三)有同学提出还可利用 pH的变化判断酸碱是否发生了反应,图 4所示是小组同学利用 pH传感器探究氢氧化钠溶液与稀盐酸反应的 pH变化曲线

(4)该反应是将_____(填序号),M 点溶液中溶质为_____(填化学式)
a.稀盐酸加入氢氧化钠溶液 b.氢氧化钠溶液加入稀盐酸
【答案】溶液由红色变为无色 NaOH+HCl=NaCl+H2O 不能 氢氧化钠固体溶于水放出热量,使集气瓶内压强增大,也会使U形管中右侧红墨水液面上升 放出 反应结束,温度逐渐恢复到室温 a NaCl
【解析】
(1)酚酞试液遇到氢氧化钠溶液变红,再加入盐酸,盐酸与氢氧化钠反应生成氯化钠和水,氢氧化钠反应完,溶液变为无色,所以可说明试管中两种物质发生反应的现象是溶液由红色变为无色;反应物是氢氧化钠和盐酸,生成物是氯化钠和水,所以方程式是:NaOH+HCl=NaCl+H2O;
(2)氢氧化钠固体溶于水放热,也能使U形管中右侧红墨水液面上升,所以仅靠观察U形管中右侧红墨水液面上升,不能判断二者发生反应;
(3)①由曲线变化情况分析可知,稀盐酸与氢氧化钠溶液发生反应并放出热量;
②400秒后,曲线开始呈下降趋势的原因是氢氧化钠与盐酸已经反应完;
(4)开始时pH>7,随着反应的进行,pH值逐渐降低,M点时pH=7,所以是向氢氧化钠中加入盐酸;M点溶液是氢氧化钠与盐酸恰好完全反应,所以溶质只有生成的氯化钠。

 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案【题目】将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)![]() 钠的氧化物
钠的氧化物![]() 氢氧化钠溶液
氢氧化钠溶液![]() 白色固体
白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:
【实验探究一】:
实验操作 | 实验现象 | 实验结论 |
取少量钠的氧化物加入足量蒸馏水 | 猜想1正确 |
【继续探究】:钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】:
实验操作 | 实验现象 | 实验结论 |
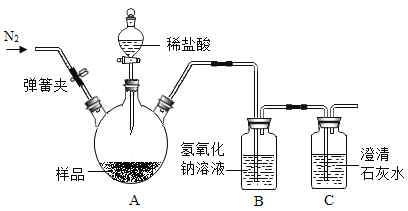
1.取少量白色固体加入足量 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
2.过滤、取少量滤液加入 |
【实验反思】
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式 。
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为 。
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2 碱性氧化物(填“是”或“不是”)。
【题目】某兴趣小组在相同条件下,将10.00g下列物质分别置于相同规格的烧杯,并敞口存放于空气中,烧杯中所有物质的质量随时间变化如下表,回答下列问题。
时间 | 质量/g | |||||
水 | 氯化钠溶液 | 盐酸 | 浓硫酸 | 氢氧化钠浓溶液 | 氯化钙溶液 | |
1天 | 8.16 | 8.62 | 8.64 | 11.18 | 9.38 | 10.25 |
2天 | 5.76 | 6.40 | 6.69 | 12.55 | 8.47 | 10.33 |
(1)图中能反映水在空气中放置时,发生变化的微观示意图是____(填标号)。
A 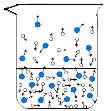 B
B 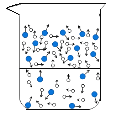 C
C 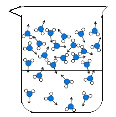 D
D 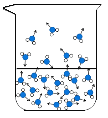
(2)为研制一种安全、环保的除湿剂,可选择上表中的____(填溶质的化学式)。
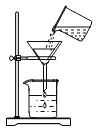
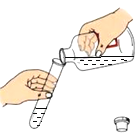
(3)为确认放置2天的盐酸浓度的变化,作如下的探究:取放置前后的盐酸分别滴入____溶液,再滴加_____相同的NaOH溶液,边滴加边振荡,当溶液颜色恰好由无色变为红色时,对比试管中溶液体积(如图所示),说明放置后盐酸溶质质量分数变____(填“大”或“小”)。

(4)氯化钠溶液放置2天后析出0.60g固体,则原氯化钠溶液是____(填“饱和溶液”或“不饱和溶液”)。(已知该温度下氯化钠的溶解度为36.0g)