题目内容
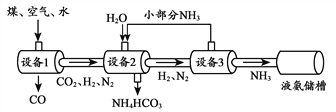
【题目】某化肥厂以煤、空气、水为原料合成氨,生产流程如下:
(1)NH3中氮元素的化合价为________________。
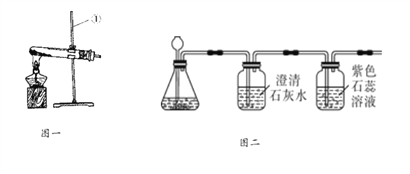
(2)设备2中参加反应的物质有______________________。
(3)设备3中发生的反应,属于基本反应类型中___________反应。
(4)该生产流程中含氮元素的物质有____________________________。
【答案】 -3 NH3、H2O、CO2 化合 空气、N2、NH3、NH4HCO3
【解析】(1)NH3中氢元素的化合价为+1,所以氮元素的化合价为-3;(2)据图进入设备2的物质有:NH3、H2O、CO2、N2、H2,剩余的物质为:N2、H2 、NH4HCO3,故设备2中参加反应的物质有:NH3、H2O、CO2;(3)设备3中发生反应后只生成NH3,故属于化合反应;(4)从图中可以看出该过程中含氮元素的物质有空气、N2、NH3、NH4HCO3。

 阅读快车系列答案
阅读快车系列答案【题目】某小组同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行探究。
【提出问题】①三种溶液的酸碱性?
②它们与酸反应时溶液的pH如何变化?
【查阅资料】
pH | 2~3 | 4~6 | 7 | 8~9 | 10~11 | 12~14 |
紫甘蓝汁液显示的颜色 | 紫红 | 浅紫 | 紫色 | 蓝色 | 绿色 | 黄色 |
【实验1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠溶液 | 氢氧化钠溶液 |
紫甘蓝汁液显示的颜色 | 紫色 | 蓝色 | 绿色 | 黄色 |
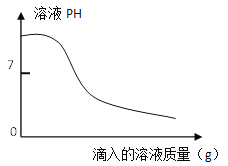
【实验2】向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图1所示。
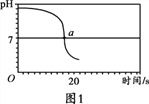
【实验3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图2、图3所示。将图2与图3的阴影部分进行叠加,发现两者基本重合。

【解释与结论】
(1)实验1得出三种溶液的碱性由强到弱的顺序为________________。
(2)实验2证明了氢氧化钠能与盐酸发生反应,其理由是_________,实验结束,向反应后的溶液中滴加紫甘蓝汁液,观察到的现象是_________。
(3)实验3中,b点的溶质为_________,c点后发生反应的化学方程式为_________。
(4)依据实验3获取的信息,鉴别Na2CO3和NaHCO3固体的实验方案为_________。