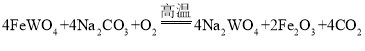题目内容
【题目】碳酸钠是生活中常见的化合物,其性质、制法是化学研究的重要内容。
(1)下列有关碳酸钠的说法不正确的是____________。
A 俗称烧碱
B 白色固体,易溶于水
C 水溶液能使石蕊溶液变蓝
D 广泛用于玻璃、造纸、纺织和洗涤剂的生产等
(2)我国化学家侯德榜发明了联合制碱法,其反应原理之一为:向饱和食盐水中先后通入足量![]() 和
和![]() ,生成小苏打(在该溶液中难溶)和一种氮肥,写出该反应的化学方程式_________。
,生成小苏打(在该溶液中难溶)和一种氮肥,写出该反应的化学方程式_________。
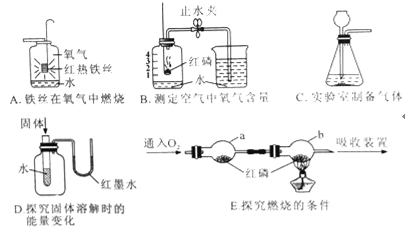
(3)实验室配制一定溶质质量分数的碳酸钠溶液的操作过程如图所示。

①实验的正确操作顺序为____________(用字母序号表示)。
②若用量筒取水时仰视读数(其它操作正确),则溶液的溶质质量分数将____________(填“偏大”、“偏小”或“不就”)。
(4)如图是某趣味实验装置图,其气密实习生良好。

①写出A装置中反应的化学方程式_________。
②C装置中可观察到什么现象_________?
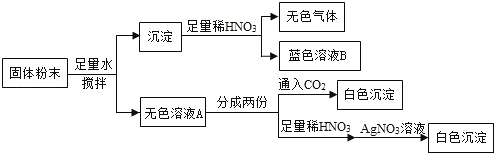
③实验结束后,若要确定D装置的溶液中溶质的成分,请设计合理的实验方案,简要写出实验步骤、现象和结论_________。
(5)某碳酸钠样品中含有少量氯化钠。为测定样品中碳酸钠的质量分数,称取6![]() 样品,加入足量水溶解,再向其中滴加澄清石灰水至沉淀不再产生,洗涤、烘干、称量后得到5
样品,加入足量水溶解,再向其中滴加澄清石灰水至沉淀不再产生,洗涤、烘干、称量后得到5![]() 沉淀。计算:该样品中碳酸钠的质量分数_________。(计算结果保留0.1%)
沉淀。计算:该样品中碳酸钠的质量分数_________。(计算结果保留0.1%)
【答案】A ![]() ECADB 偏小
ECADB 偏小 ![]() 有气泡产生 取少量D装置中的溶液,加入足量
有气泡产生 取少量D装置中的溶液,加入足量![]() 溶液(或
溶液(或![]() 溶液等)静置,取上层清液,向其中滴加几滴酚酞溶液。若溶液变成红色,则溶质为
溶液等)静置,取上层清液,向其中滴加几滴酚酞溶液。若溶液变成红色,则溶质为![]() 和
和![]() ;若溶液没有变成红色,则溶质为
;若溶液没有变成红色,则溶质为![]() 88.3%
88.3%
【解析】
(1)碳酸钠俗称纯碱、苏打,不是烧碱,故A不正确。
B、碳酸钠是白色的固体,故正确;
C、碳酸钠溶液显碱性,故能使石蕊溶液变蓝,故正确;
D、碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产等,故正确。故选A。
(2)反应物是氯化钠、水、氨气、二氧化碳,生成物是碳酸氢钠和氯化铵,再根据化学方程式的书写方程式为:![]() 。
。
(3)①配制溶液的步骤为:计算、称量(量取)、溶解,故正确的操作顺序为ECADB;
②用量筒量取水时,若读数时俯视,则读数比实际液体体积小,会造成实际量取的水的体积偏大,则会造成溶液的溶质质量分数偏小
(4)①过氧化氢在过氧化锰的催化作用下分解生成水和氧气,反应的方程式为:![]() ;②A装置中的过氧化氢分解生成氧气,使B装置内的压强增大,将稀盐酸压入C装置中,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,故C装置中可观察到气泡产生的现象;③C装置中生成的二氧化碳和D装置中的氢氧化钠反应生成碳酸钠和水,故D装置的溶液中一定含有碳酸钠,可能还含有氢氧化钠,由于碳酸钠和氢氧化钠都显碱性,故要检验氢氧化钠需要先加入足量
;②A装置中的过氧化氢分解生成氧气,使B装置内的压强增大,将稀盐酸压入C装置中,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,故C装置中可观察到气泡产生的现象;③C装置中生成的二氧化碳和D装置中的氢氧化钠反应生成碳酸钠和水,故D装置的溶液中一定含有碳酸钠,可能还含有氢氧化钠,由于碳酸钠和氢氧化钠都显碱性,故要检验氢氧化钠需要先加入足量![]() 溶液(或
溶液(或![]() 溶液等)检验并除去碳酸钠。
溶液等)检验并除去碳酸钠。
(5)设6![]() 样品碳酸钠的质量为
样品碳酸钠的质量为![]() 。
。

![]()
![]()
样品中碳酸钠的质量分数为:![]()
答:该样品中碳酸钠的质量分数为88.3%。